题目内容
下列反应的离子方程式正确的是
A.铜片加入三氯化铁溶液中:Cu+2Fe3+=2Fe2++Cu2+
B.盐酸中加入碳酸钙:CO32-+2H+=H2O+CO2↑
C.AlCl3溶液中加入足量的氨水:Al3++3OH-=Al(OH)3↓
D.NaHCO3溶液中加入盐酸:CO32-+2H+=H2O+CO2↑
A
【解析】
试题分析:A、符合离子方程式的书写原则,正确;B、碳酸钙是难溶物,不能拆开,错误;C、一水合氨是弱碱,不能写成氢氧根离子,错误;D、碳酸氢根离子不能写成碳酸根离子形式,错误,答案选A。
考点:考查离子方程式的书写

练习册系列答案
相关题目
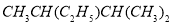 的名称是 。
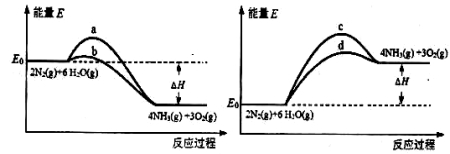
的名称是 。 2NH3
2NH3 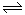 4NH3(g)+3O2(g) △H=Q ①
4NH3(g)+3O2(g) △H=Q ①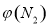 与反应温度T的关系曲线如下图所示,则上述反应的Q________0(填“>”、“<”或“=”)。
与反应温度T的关系曲线如下图所示,则上述反应的Q________0(填“>”、“<”或“=”)。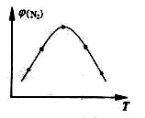
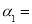 ______________。
______________。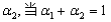 时,则起始时NH3的物质的量
时,则起始时NH3的物质的量 _________mol。
_________mol。