题目内容
下列叙述中正确的是
A.相同条件下,N2和O3混合气与等体积的N2所含原子数相等
B.等物质的量的甲基(—CH3)和羟基(—OH)所含电子数相等
C.常温常压下28 g CO与22.4 L O2所含分子数相等
D.16g CH4与18 g NH4+ 所含质子数相等
【答案】
B
【解析】
试题分析:本题是对物质的量以及阿伏伽德罗常数的综合应用。
选项A、因N2和O3中分子所含有的原子个数不同,因此“N2和O3混合气与等体积的N2所含原子数不相等”;
选项B、正确。一个甲基(—CH3)和羟基(—OH)所含电子数均为10个,因此等物质的量的甲基(—CH3)和羟基(—OH)所含电子数相等;
选项C、常温常压下28 g CO的物质的量为1mol,而在常温常压下,22.4 L O2的物质的量不为1mol,故选项C说法错误;
选项D、16g CH4所含有的质子数为10mol,18 g NH4+ 所含质子数为11mol,二者所含的质子数不相等。
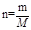 考点:化学计量的综合应用
考点:化学计量的综合应用
点评:对化学计量的考查,首先需掌握有关化学计量计算的基本公式。如:
1、对于粒子数目的计算,实际上是算“物质的量”,物质的量相等,其粒子数目必定相等。
2、对于粒子中质子数的计算:“质子数=核电荷数=电子数=原子序数”,一个粒子的总质子数等于所有原子的原子序数(即质子数)之和。如CH4的质子数=6×1﹢1×4=10.

练习册系列答案
相关题目
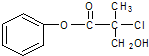 有机物A是农药生产中的一种中间体,结构简式如图所示.下列叙述中正确的是( )
有机物A是农药生产中的一种中间体,结构简式如图所示.下列叙述中正确的是( )| A、有机物A可以在一定条件下与HBr发生反应 | B、1mol A最多能与4mol H2发生加成反应 | C、有机物A与浓硫酸混合加热,可以发生消去反应 | D、1mol A与足量的NaOH溶液反应,最多可以消耗3mol NaOH |


