题目内容
2.(1)①实验室常用MnO2制备Cl2,反应的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.若反应中消耗的MnO2为87g,则被氧化的HCl为73g.②下列收集Cl2的方法正确的是C(填字母)

③用如图装置进行实验,甲中红色布条褪色,丙中红色布条不褪色,则乙中的试剂是浓硫酸.

(2)ClO2是公认的最安全的消毒剂,现在可以用如下反应制备ClO2,
1H2C2O4+2NaClO3+1H2SO4═1Na2SO4+2CO2↑+2ClO2↑+2H2O,配平该反应,并用单线桥法表示电子转移情况.
(3)家用84消毒液的主要成分是NaClO,其若和洁厕灵(主要成分是盐酸)一起使用生成有毒的气体,反应的离子方程式为ClO-+Cl-+2H+=Cl2↑+H2O.
分析 (1)①实验室常用MnO2制备Cl2,反应的化学方程式为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ MnCl2+Cl2↑+2H2O,MnO2完全反应,根据n=$\frac{m}{M}$计算87g的MnO2的物质的量,求被氧化的HCl;
②氯气易溶于水,与水反应且比空气大且密度有毒,所以收集Cl2用向上排空气法,并有尾处理装置;
③用如图装置进行实验,甲中红色布条褪色,丙中红色布条不褪色,说明进入丙中的气体被干燥;
(2)根据得失电子守恒和物料守恒分析可得:H2C2O4+2NaClO3+H2SO4═Na2SO4+2CO2↑+2ClO2↑+2H2O,单线桥法表示电子转移情况是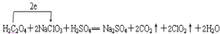 ;
;
(3)家用84消毒液的主要成分是NaClO,其若和洁厕灵(主要成分是盐酸)一起使用生成有毒的气体是氯气,反应的离子方程式为ClO-+Cl-+2H+=Cl2↑+H2O.
解答 解:(1)①实验室常用MnO2制备Cl2,反应的化学方程式为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ MnCl2+Cl2↑+2H2O,MnO2完全反应,MnO2的物质的量n=$\frac{m}{M}$=$\frac{87g}{87g/mol}$=1mol,所以被氧化的盐酸是2mol,质量为:2mol×36.5g/mol=73g,故答案为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ MnCl2+Cl2↑+2H2O;73;
②氯气易溶于水,与水反应且比空气大且密度有毒,所以收集Cl2用向上排空气法,并有尾处理装置,故选C;
③用如图装置进行实验,甲中红色布条褪色,丙中红色布条不褪色,说明进入丙中的气体被干燥,故答案为:浓硫酸;
(2)根据得失电子守恒和物料守恒分析可得:H2C2O4+2NaClO3+H2SO4═Na2SO4+2CO2↑+2ClO2↑+2H2O,单线桥法表示电子转移情况是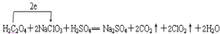 ,故答案为:1、2、1、1、2、2、2;
,故答案为:1、2、1、1、2、2、2;
(3)家用84消毒液的主要成分是NaClO,其若和洁厕灵(主要成分是盐酸)一起使用生成有毒的气体是氯气,反应的离子方程式为ClO-+Cl-+2H+=Cl2↑+H2O,故答案为:ClO-+Cl-+2H+=Cl2↑+H2O.
点评 本题考查根据方程式计算、氧化还原反应计算和氯气性质的实验等,比较基础,注意基础知识的理解掌握.

| A. | 3.2 g | B. | 4.8 g | C. | 5.4 g | D. | 3.8 g |
| 序号 | 物质 | 杂质 | 除杂质所选用的试剂或操作方法 |
| A | Mg | Al | 加入过量盐酸溶液,充分反应,过滤 |
| B | NaHCO3溶液 | Na2CO3溶液 | 加入足量氢氧化钡溶液,充分反应,过滤 |
| C | NO | NO2 | 通过盛有水的洗气瓶,再干燥 |
| D | FeCl3溶液 | FeCl2溶液 | 加入过量的铁粉,充分反应,过滤 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 常温常压下,14gN2含有的分子数为0.5NA | |
| B. | 标准状况下,11.2LH2O含有的分子数为0.5NA | |
| C. | 0.1mol•L-1的NaOH溶液中含钠离子数为0.1NA | |
| D. | 1.8gNH4+中含有的电子数为0.1NA |
| A. | 从分子中碳骨架形状分:异丁烷为链状有机化合物,甲苯为环状有机化合物 | |
| B. | 蒸馏常用于分离提纯液态有机混合物 | |
| C. | 核磁共振氢谱通常用于分析有机物的相对分子质量 | |
| D. | 对有机物分子红外光谱图的研究有助于确定有机物分子中的官能团 |
| A. | 0.1mol/L的NH4Cl溶液:c(Cl-)>c(NH4+)>c(OH-)>c(H+) | |
| B. | 0.1mol/L的CH3COOH溶液:c(CH3COOH)>c(H+)>c(CH3COO-)>c(OH-) | |
| C. | pH=4的FeCl3溶液:c(Cl-)>c(H+)>c(Fe3+)>c(OH-) | |
| D. | pH=11的CH3COONa溶液:c(Na+)+c(H+)=c(CH3COO-)+c(CH3COOH) |



