题目内容
下列有关说法不正确的是( )
| A、高容量储氢材料的研制是推广应用氢氧燃料电池的关键问题之一 |
| B、发展低碳经济,推广可利用太阳能的城市照明系统有利于节能减排、改善环境质量 |
| C、仅需要托盘天平、砝码、药匙、一定规格的容量瓶、烧杯、玻璃棒这些仪器就可以准确配制出一定浓度的NaCL溶液 |
| D、节日燃放的焰火是某些金属元素焰色反应所呈现出来的色彩 |
考点:原电池和电解池的工作原理,常见的生活环境的污染及治理,焰色反应
专题:基本概念与基本理论,元素及其化合物
分析:A.氢气难以液化和储存;
B.太阳能电池为清洁能源;
C.缺少胶头滴管;
D.焰色反应可用于烟花.
B.太阳能电池为清洁能源;
C.缺少胶头滴管;
D.焰色反应可用于烟花.
解答:
解:A.氢气难以液化和储存,氢氧燃料电池的负极为氢气的氧化反应,则负极应为高容量储氢材料,为研制燃料电池的关键技术,是推广应用氢氧燃料电池的关键问题之一,故A正确;
B.太阳能电池为清洁能源,有利于节能减排、改善环境质量,故B正确;
C.缺少胶头滴管,难以完成实验,故C错误;
D.不同金属的焰色反应的颜色不同,焰色反应可用于烟花,故D正确.
故选C.
B.太阳能电池为清洁能源,有利于节能减排、改善环境质量,故B正确;
C.缺少胶头滴管,难以完成实验,故C错误;
D.不同金属的焰色反应的颜色不同,焰色反应可用于烟花,故D正确.
故选C.
点评:本题考查较为综合,涉及燃料电池、能源、溶液的配制以及焰色反应的应用等问题,侧重于化学与生活的考查,有利于培养学生良好的科学素养,提高学习的积极性,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
某同学设计了由乙醇合成乙二醇的路线如下.下列说法正确的是( )
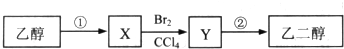

| A、X可以发生加成反应 |
| B、步骤①的反应类型是水解反应 |
| C、步骤②需要在氢氧化钠醇溶液中反应 |
| D、等物质的量的乙醇、X完全燃烧,消耗氧气的量不相同 |
用下列方法制取氢气,反应速率最大的是( )
| A、10℃时,粉末状锌与2mol?L-1硫酸溶液反应 |
| B、30℃时,粉末状锌与2mol?L-1硫酸溶液反应 |
| C、10℃时,块状锌与2mol?L-1硫酸溶液反应 |
| D、30℃时,块状锌与2mol?L-1硫酸溶液反应 |
甲酸的下列性质中,可以证明它是弱电解质的是( )
| A、甲酸能与水以任意比互溶 |
| B、1mol/L甲酸溶液的PH约为2 |
| C、10mL1mol/L甲酸恰好与10mL1mol/LNaOH溶液完全反应 |
| D、在相同条件下,甲酸溶液的导电性比强酸溶液的弱 |
下列物质中,不能与金属钠反应放出氢气的是( )
| A、苯 | B、水 | C、乙醇 | D、乙酸 |
使用容量瓶配置溶液时,由于操作不当会引起误差,下列情况会使所配溶液浓度偏低的是( )
①用天平称量时所用砝码生锈
②用量筒量取所需浓溶液时,仰视刻度
③溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤
④转移溶液前容量瓶内有少量蒸馏水
⑤定容时,俯视容量瓶的刻度线
⑥定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线.
①用天平称量时所用砝码生锈
②用量筒量取所需浓溶液时,仰视刻度
③溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤
④转移溶液前容量瓶内有少量蒸馏水
⑤定容时,俯视容量瓶的刻度线
⑥定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线.
| A、②⑤ | B、②③⑥ |
| C、①⑤⑥ | D、③⑥ |
已知:C(s)+H2O(I)=CO(g)+H2(g)△H1═+175.3kJ/mol
CO(g)+
O2(g)═CO2(g)△H2═-283.0kJ/mol
H2(g)+
O2(g)═H2O(Ⅰ)△H3═-283.0kJ/mol
则C(s)+O2(g)═CO2(g)的△H等于( )
CO(g)+
| 1 |
| 2 |
H2(g)+
| 1 |
| 2 |
则C(s)+O2(g)═CO2(g)的△H等于( )
| A、390.7kj/mol |
| B、-679.3kj/mol |
| C、-787kj/mol |
| D、+180.9kj/mol |
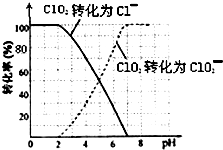 二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂.比Cl2更好.
二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂.比Cl2更好.