题目内容
下列变化中一定为放热的化学反应的是

A.H2O(g)===H2O(l) ΔH=-44.0 kJ·mol-1
B.N2(g)+O2(g)===2NO(g) ΔH=+182.6 kJ·mol-1
C.形成化学键过程中放出862 kJ热量的化学反应
D.能量变化如上图所示的化学反应
D
【解析】
试题分析:A、H2O(g)===H2O(l) ΔH=-44.0 kJ?mol-1 不是化学反应,A错误;B、N2(g)+O2(g)===2NO(g) ΔH=+182.6 kJ?mol-1 焓变为正是吸热反应,B错误;C、形成化学键过程中放出862 kJ热量的化学反应,断裂化学键吸收热量,不能确定反应放热还是吸热,C错误;D、能量变化如图所示的化学反应,反应物的能量高,生成物的能量低,反应放热,D正确;答案选D。
考点:反应热图像

练习册系列答案
相关题目
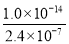 mol·L-1 D.无法确定
mol·L-1 D.无法确定