题目内容
某溶液中,25℃时由水电离产生的[H+]=1×10-11mol·L-1,则该溶液的pH可能为
[ ]
A.11
B.3
C.9
D.7
答案:AB
解析:
提示:
解析:
|
【巧解导析】在稀酸稀碱溶液,[H+]水=[OH-]水,而溶液[H+]·[OH-]=10-14(25℃),显然此溶液中水的电离受到抑制,该溶液可能为酸溶液,也可能为碱溶液,应分两种情况讨论: 若为酸溶液,则溶液中的OH-全部是由水电离出,且[OH-]=[H+]水=10-11mol·L-1,溶液中的总H+浓度为:[H+] 若为碱溶液,则溶液中的H+全部是由水电离产生,且[H+]=[H+]水=10-11mol·L-1,溶液中的[OH-]= |
提示:
|
【巧解点悟】解题关键点是要抓住溶液中[H+]与[OH-]之间的关系,灵活运用KW.解题易错点为:若忽视酸、碱对水电离平衡的影响则易选D;若思考问题不全面则易漏选A或B. |

练习册系列答案
相关题目
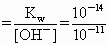 =10-3mol·L-1,则溶液pH=3.
=10-3mol·L-1,则溶液pH=3.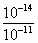 =10-3mol·L-1,此时由pH的定义式知:pH=-lg[H+]=11.
=10-3mol·L-1,此时由pH的定义式知:pH=-lg[H+]=11.