题目内容
自2010年8月7日,甘肃省舟曲县发生特大泥石流后,各地的救援物资源源不断运往灾区.下图为地方捐助的一种国家准字号补铁补血用药--复方硫酸亚铁叶酸片,其主要成分是绿矾--硫酸亚铁晶体(FeSO4?7H2O).
某校课外活动小组为测定该补血剂中铁元素的含量特设计实验步骤如下:
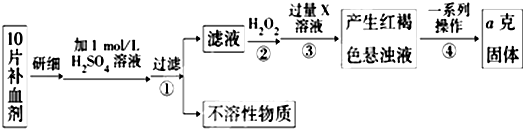
请回答下列问题:
(1)步骤②中加入过量H2O2的目的是 .
(2)步骤③中反应的离子方程式为 .
(3)步骤④中一系列处理的操作步骤是:过滤、 、灼烧、 、称量.
(4)若实验无损耗,则每片补血剂含铁元素的质量为 g(用含a的代数式表示).
(5)用稀硫酸酸化的KMnO4溶液也能氧化Fe2+的水溶液,KMnO4被还原为Mn2+,请写出此反应的离子方程式: .
某校课外活动小组为测定该补血剂中铁元素的含量特设计实验步骤如下:

请回答下列问题:
(1)步骤②中加入过量H2O2的目的是
(2)步骤③中反应的离子方程式为
(3)步骤④中一系列处理的操作步骤是:过滤、
(4)若实验无损耗,则每片补血剂含铁元素的质量为
(5)用稀硫酸酸化的KMnO4溶液也能氧化Fe2+的水溶液,KMnO4被还原为Mn2+,请写出此反应的离子方程式:
考点:探究物质的组成或测量物质的含量
专题:实验探究和数据处理题
分析:由流程图可知,该实验原理为:将药品中的Fe2+形成溶液,将Fe2+氧化为Fe3+,使Fe3+转化为氢氧化铁沉淀,再转化为氧化铁,通过测定氧化铁的质量,计算补血剂中铁元素的含量.
(1)双氧水具有氧化性,酸性条件下能将Fe2+全部氧化为Fe3+,由流程图可知,加入H2O2是将Fe2+氧化为Fe3+;
(2)步骤③是将Fe3+转化为氢氧化铁沉淀;
(3)氢氧化铁沉淀过滤、洗涤、干燥,可以得到氢氧化铁固体,灼烧、冷却称量,得到一定质量的氧化铁;
(4)根据铁元素守恒可知ag氧化铁中铁元素的质量即为10片补血剂中铁的质量,据此计算;
(5)根据题给信息,写出反应的离子方程式.
(1)双氧水具有氧化性,酸性条件下能将Fe2+全部氧化为Fe3+,由流程图可知,加入H2O2是将Fe2+氧化为Fe3+;
(2)步骤③是将Fe3+转化为氢氧化铁沉淀;
(3)氢氧化铁沉淀过滤、洗涤、干燥,可以得到氢氧化铁固体,灼烧、冷却称量,得到一定质量的氧化铁;
(4)根据铁元素守恒可知ag氧化铁中铁元素的质量即为10片补血剂中铁的质量,据此计算;
(5)根据题给信息,写出反应的离子方程式.
解答:
解:测定该补血剂中铁元素的含量,由流程可知,溶解后过滤除杂不溶性杂质,滤液中加过氧化氢将亚铁离子氧化为铁离子,再与过量氨水反应生成氢氧化铁沉淀,过滤、洗涤、灼烧、冷却后称量得到氧化铁的质量,
(1)步骤②加入过量H2O2的目的将亚铁离子全部氧化为铁离子,故答案为:把Fe2+ 氧化为Fe3+;
(2)步骤③中加入X可为氢氧化钠,反应的离子方程式为Fe3++3 OH-═Fe (OH)3↓;
故答案为:Fe3++3 OH-═Fe (OH)3↓;
(3)步骤④中一系列处理的操作步骤:过滤、洗涤、灼烧、冷却、称量,故答案为:洗涤;冷却;
(4)ag为氧化铁的质量,10片中含铁元素的质量为ag×
×100%=0.7ag,每片补血剂含铁元素的质量0.07ag,故答案为:0.07a;
(5)用稀硫酸酸化的KMnO4溶液也能氧化Fe2+的水溶液,KMnO4被还原为Mn2+,则反应物为MnO4-、Fe2+和H+,生成物为Fe3+、Mn2+和水,配平离子方程式为:MnO4-+5Fe2++8 H+═Mn2++5Fe3++4H2O,
故答案为:MnO4-+5Fe2++8H+═Mn2++5Fe3++4H2O.
(1)步骤②加入过量H2O2的目的将亚铁离子全部氧化为铁离子,故答案为:把Fe2+ 氧化为Fe3+;
(2)步骤③中加入X可为氢氧化钠,反应的离子方程式为Fe3++3 OH-═Fe (OH)3↓;
故答案为:Fe3++3 OH-═Fe (OH)3↓;
(3)步骤④中一系列处理的操作步骤:过滤、洗涤、灼烧、冷却、称量,故答案为:洗涤;冷却;
(4)ag为氧化铁的质量,10片中含铁元素的质量为ag×
| 56×2 |
| 160 |
(5)用稀硫酸酸化的KMnO4溶液也能氧化Fe2+的水溶液,KMnO4被还原为Mn2+,则反应物为MnO4-、Fe2+和H+,生成物为Fe3+、Mn2+和水,配平离子方程式为:MnO4-+5Fe2++8 H+═Mn2++5Fe3++4H2O,
故答案为:MnO4-+5Fe2++8H+═Mn2++5Fe3++4H2O.
点评:本题考查物质含量的测定,为高频考点,把握测定原理及实验流程中的反应、混合物分离方法等为解答的关键,侧重分析与实验、计算能力的综合考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列反应所产生的气体体积在标准状况下为22.4L的是( )
| A、将2mol金属Cu与含2molH2SO4的浓硫酸共热 |
| B、将1 mol MnO2固体与含4molHCl的浓盐酸共热 |
| C、常温下,将32.2g金属钠和5.4g金属铝同时投入到足量水中 |
| D、常温下,将10.8g的Al和22.4g的Fe投入到300g 98%的硫酸中 |
下列有关物质用途的说法正确的是( )
| A、单质硅常用做半导体材料和光导纤维,SiO2是人类将光能转化为电能的常用材料 |
| B、纯碱、烧碱、Al(OH)3等常用于治疗胃酸过多 |
| C、H2O2、Na2O2、氯水、漂白粉、84消毒液均可作漂白剂和消毒剂,且它们的漂白原理相同 |
| D、镁铝合金常用于制作窗框是因为它具有坚硬、密度小、溶点高、耐腐蚀等优良性能 |
为除去括号内的杂质,所选用的试剂或方法不正确的是( )
| A、Na2CO3溶液(Na2SO4),加入适量的Ba(OH)2溶液,过滤 |
| B、NaHCO3溶液(Na2CO3),应通入过量的CO2气体 |
| C、Na2O2粉末(Na2O),将混合物在氧气中加热 |
| D、Na2CO3溶液(NaHCO3),选用适量的NaOH溶液 |


 )
)
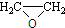 ).写出以邻甲基苯酚(
).写出以邻甲基苯酚(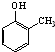 )和乙醇为原料制备
)和乙醇为原料制备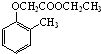 的合成路线流程图(无机试剂任用).
的合成路线流程图(无机试剂任用).
