题目内容
1.某强氧化剂[RO(OH)2]+能将Na2SO3氧化.已知含4.0×10-3mol[RO(OH)2]+离子的溶液,恰好跟25.0mL 0.4mol•L-1,的Na2SO3,溶液完全反应,则反应后R的化合价为0价.分析 [RO(OH)2]+离子中R的化合价为+5价,将Na2SO3氧化生成Na2SO4,令R元素在还原产物中化合价为a,结合氧化还原反应中氧化剂和还原剂得失电子数目计算.
解答 解:Na2SO3被氧化后生成Na2SO4,
[RO(OH)2]+离子中R的化合价为+5价,设还原后的化合价为a,
由电子转移守恒可知:0.025L×0.4mol/L×(6-4)=4.0×10-3mol×(5-a),
解得a=0,
故答案为:0.
点评 本题考查氧化还原反应的计算,为高考常见题型,侧重于学生的分析能力和计算能力的考查,注意从电子转移守恒角度解答,题目难度不大.

练习册系列答案
 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案
相关题目
11.一定温度下,对于可逆反应A2(g)+3B2(g)?2AB3(g)(正反应放热)的下列叙述,不能说明反应已达化学平衡状态的是( )
| A. | 恒容容器内混合气体的密度不再变化 | |
| B. | AB3的生成速率与B2的生成速率之比为2:3 | |
| C. | 恒压容器内混合气体的总物质的量不再变化 | |
| D. | 单位时间内断裂a mol A≡A键,同时断裂6a mol A-B键 |
12.合理、丰富的营养是健康的保证.2004年安徽阜阳出现的“大头娃娃”事件就是因婴儿吃了缺乏营养成分的劣质奶粉造成的.下列物质中不属营养物质的是( )
| A. | 油脂 | B. | 阿司匹林 | C. | 矿物质 | D. | 维生素 |
9.有关化学平衡常数(K)的说法中不正确的是( )
| A. | 一般地说,K>105时,该反应进行得就基本完全了 | |
| B. | 对一个确定的反应,K值越大,正反应进行的程度越大 | |
| C. | 在温度一定时,K与反应物或生成物的浓度变化无关 | |
| D. | 温度越高,K值越大 |
16.NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 常温下,1 mol•L-1的NH4NO3溶液中含有氮原子的数目为2 NA | |
| B. | 22.4L氯气通入足量氢氧化钠溶液中充分反应,转移的电子数为NA | |
| C. | 标准状况下,5.6 L四氯化碳含有的分子数为0.25NA | |
| D. | 4.6gNa完全转化成Na2O和Na2O2的混合物,生成物中阴离子总数为0.1NA |
6.下列设计的实验方案能达到实验目的是( )
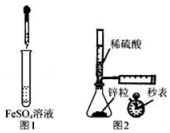

| A. | 制备Fe(OH)2:用图1所示装置,向试管中加入NaOH溶液,振荡 | |
| B. | 测定H2的生成速率:用图2所示装置,制取一定体积的H2,记录时间 | |
| C. | 中和热测定实验中把盐酸分多次加入氢氧化钠溶液中 | |
| D. | 酸碱中和滴定实验中锥形瓶需要用待测液润洗 |
13.下列各组离子中,因发生氧化还原反应而不能大量共存的是( )
| A. | K+、H+、Fe2+、MnO4- | B. | Fe3+、Ba2+、SO42-、NO3- | ||
| C. | Al3+、Na+、SO42-、CO32- | D. | Fe3+、H+、SO42-、ClO- |