题目内容
16.下列物质一定属于同系物的是( )①
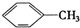 ②
②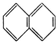 ③
③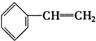 ④C2H4
④C2H4⑤CH2═CH-CH═CH2 ⑥C3H6 ⑦
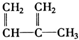 ⑧
⑧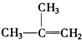
| A. | ①和② | B. | ④和⑥ | C. | ④和⑧ | D. | ⑦和⑧ |
分析 结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称为同系物;互为同系物的物质满足以下特点:结构相似、化学性质相似、分子式通式相同、分子式不同,研究对象是有机物,注意如果含有官能团,则官能团的种类及数目必须完全相同.
解答 解:A.①为甲苯,②为萘,二者含苯环个数不同,一定不属于同系物,故A错误;
B.④为乙烯,分子中含有碳碳双键,而⑥可能为环丙烷或丙烯,二者结构不一定相似,所以二者不一定互为同系物,故B错误;
C.④为乙烯,分子中含有碳碳双键,而⑧为2-甲基-1-丙烯,二者都是烯烃,分子结构相似,分子间相差2个CH2原子团,所以④⑧一定属于同系物,故C正确;
D.⑦为2-甲基-1.3-丁二烯,而⑧为2-甲基-1-丙烯,二者含官能团数目不同,所以⑦⑧一定不是同系物,故D错误;
故选C.
点评 本题考查了同系物的判断,题目难度不大,注意掌握常见有机物结构与性质,明确同系物的概念及判断方法,特别注意互为同系物的有机物,如果含有官能团时,官能团的类型及数目必须相同.

练习册系列答案
相关题目
6.如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22.下列说法正确的是( )
| X | Y | ||
| W | Z | ||
| T |
| A. | X、Y、Z三种元素最低价氢化物的沸点依次升高 | |
| B. | T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ4 | |
| C. | 由X、Y和氢三种元素形成的化合物中只有共价键 | |
| D. | 物质WY2、W3X4、WZ4均有熔点高、硬度小的特性 |
11.下列各物质中,不能发生水解反应的是( )
| A. | 油脂 | B. | 果糖 | C. | 氨基酸 | D. | 淀粉 |
1.为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题.
(1)过氧化氢分解的化学方程式为2H2O2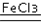 2H2O+O2↑.
2H2O+O2↑.
(2)实验①的目的是研究温度对H2O2分解速率的影响.
(3)实验②未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是将两支试管同时放入盛有相同温度热水的烧杯中,或向两支试管中同时滴入2滴1mol/L FeCl3溶液,观察产生气泡的速率 (用实验中提供的试剂).
(4)对于H2O2分解反应,Cu2+也有一定的催化作用.为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验.请回答相关问题:
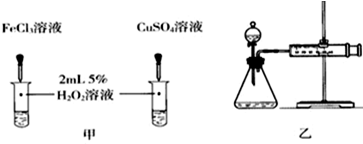
①定性分析:如图甲可通过观察溶液中气泡产生的速率,定性比较得出结论.有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是控制阴离子相同,排除阴离子的干扰.
| 编号 | 操作 | 实验现象 |
| ① | 分别在试管A、B中加入5mL 5% H2O2溶液,各滴入2滴等浓度 FeCl3溶液.待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中浸泡;将试管B放入盛有40℃左右热水的烧杯中浸泡. | 试管A中不再产生气泡;试管B中产生的气泡量增大. |
| ② | 另取两支试管分别加入5mL 5% H2O2溶液和5mL 10% H2O2溶液 | 试管A、B中均未明显见到有气泡产生. |
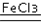 2H2O+O2↑.
2H2O+O2↑.(2)实验①的目的是研究温度对H2O2分解速率的影响.
(3)实验②未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是将两支试管同时放入盛有相同温度热水的烧杯中,或向两支试管中同时滴入2滴1mol/L FeCl3溶液,观察产生气泡的速率 (用实验中提供的试剂).
(4)对于H2O2分解反应,Cu2+也有一定的催化作用.为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验.请回答相关问题:

①定性分析:如图甲可通过观察溶液中气泡产生的速率,定性比较得出结论.有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是控制阴离子相同,排除阴离子的干扰.
8.如图所示,通电后A极上析出Ag,对该装置的有关叙述正确的是( )
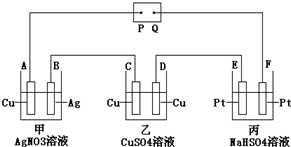

| A. | P是电源的正极 | |
| B. | F极上发生的反应为:4OH--4e-=2H2O+O2↑ | |
| C. | 电解时,甲、乙、丙三池中,除E、F两极外,其余电极均参加了反应 | |
| D. | 通电后,甲池溶液的pH减小,乙池溶液的浓度增大、丙池溶液的pH不变 |
5.下列有关化学反应速率和化学平衡的说法正确的是( )
| A. | 可逆反应达到化学平衡状态时,正、逆反应速率均等于零 | |
| B. | 当反应物与生成物浓度相等时,可逆反应一定已达到化学平衡 | |
| C. | 化学反应的限度决定了反应物在该条件下的最大转化率 | |
| D. | 镀锌铁制品镀层受损后,铁制品比受损前更易生锈 |
15.下列化学反应中,既有离子键、极性键、非极性键断裂,又有离子键、极性键、非极性键形成的是( )
| A. | 2Na2O2+2H2O═4NaOH+O2↑ | B. | Mg3Cl2+2NaOH═Mg(OH)2↓+2NaCl | ||
| C. | 2NaOH+Cl2═NaOCl+H2O | D. | NH4Cl+NaO═NaCl+NH3↑+H2O |
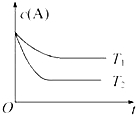 反应A(g)?B(g)+C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol•L-1.温度T1和T2下A的浓度与时间关系如图所示.回答下列问题:
反应A(g)?B(g)+C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol•L-1.温度T1和T2下A的浓度与时间关系如图所示.回答下列问题: