题目内容
12.将一定质量由Cu和CuO组成的固体粉末加入到100mL 11mol•L-1的浓HNO3中,充分反应后,固体溶解完全,收集到NO、NO2混合气体6.72L(标准状况).若将该混合气体与2.24L O2(标准状况)混合并通入到足量水中,恰好生成HNO3.(1)NO的体积是1.12L(标准状况).
(2)固体粉末中Cu单质的质量是12.8g.
(3)向浓HNO3反应后的溶液中加入4mol•L-1的NaOH溶液,当Cu2+恰好沉淀完时,需要NaOH溶液的体积是0.2L.
分析 (1)铜和浓硝酸反应生成二氧化氮,和稀硝酸反应生成NO,根据转移电子守恒计算二氧化氮和NO的物质的量,然后计算体积;
(2)根据得失电子守恒,n(Cu)=2n(O2),计算求解;
(3)向反应后溶液中加入NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,此时溶液中溶质为NaNO3,由钠离子守恒n(NaNO3)=n(NaOH),根据氮原子守恒可知n(HNO3)=n(NaNO3)+n(NO2+NO),最后根据V=$\frac{n}{c}$计算出需要氢氧化钠溶液的体积.
解答 解:铜与浓硝酸反应的化学方程式为:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,铜与稀硝酸反应的化学方程式为:3Cu+8HNO3(稀)=3Cu(NO3)2+NO↑+4H2O,
设生成的NO的物质的量为xmol,NO2的物质的量为ymol,反应中铜失去的电子总数等于硝酸得到的电子总数则
Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
1 4 2
0.5y 2y y
3Cu+8HNO3(稀)=3Cu(NO3)2+NO↑+4H2O
3 8 1
3x 8x x
根据生成NO、NO2的物质的量可知:x+y=$\frac{6.72L}{22.4L/mol}$、根据电子守恒可知:3×x+y×1=$\frac{2.24L}{22.4L/mol}$×4,
联立解得:x=0.05mol、y=0.25mol,
(1)生成的NO的体积为:0.05mol×22.4mol/L=1.12L,
故答案为:1.12;
(2)n(Cu)=2n(O2)=0.2mol,所以m(Cu)=0.2mol×64g/mol=12.8g,
故答案为:12.8;
(3)依据氮原子个数守恒得,硝酸的物质的量=n(NaNO3)+n(NO2+NO)=0.1×11mol,所以n(NaNO3)=1.1-0.3=0.8mol,所以氢氧化钠的物质的是0.8mol,所以体积为:V=$\frac{0.8mol}{4mol/L}$=0.2mol,
故答案为:0.2.
点评 本题考查混合物反应的计算,题目难度中等,侧重于学生的分析能力和计算能力的考查,明确反应实质为解答关键,注意结合方程式利用原子守恒进行的计算,试题培养了学生的化学计算能力.

 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案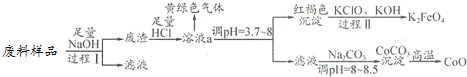
(1)过程Ⅰ中的操作名称是过滤,写出过程Ⅰ发生反应的化学方程式Al2O3+2NaOH═2NaAlO2+H2O.
(2)溶液a中含有金属离子有Co2+、Fe3+.
(3)溶液a中逸出的黄绿色气体是氯气,下列说法不正确的是①、④.
①氯气是有漂白性的酸性气体
②液氯和氯水均为液体,且都含有氯分子
③将氯气通入碱液时,氯气既是氧化剂,又是还原剂
④次氯酸见光易分解,说明次氯酸是弱酸
⑤向氯水中滴硝酸银溶液,有白色沉淀生成,说明氯水中含Cl-
(4)写出过程Ⅱ发生反应的离子方程式:2Fe(OH)3+3ClO-+4OH-═2FeO42-+5H2O+3Cl-.
高铁电池的总反应为:3Zn+2K2FeO4+8H2O$?_{充电}^{放电}$3Zn(OH)2+2Fe(OH)3+4KOH
则充电时阳极反应式为Fe(OH)3-3e-+5OH-═FeO42-+4H2O.
(5)Co可以形成CoC2O4•2H2O(M为183g/mol),5.49g该晶体在空气中加热,在不同温度下分别得到一种固体物质,其质量如表:
| 温度范围(℃) | 固体质量(g) |
| 150-210 | 4.41 |
| 290-320 | 2.41 |
| 890-920 | 2.25 |
| A. | 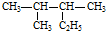 按系统命名法的名称为:2-甲基-3-乙基丁烷 按系统命名法的名称为:2-甲基-3-乙基丁烷 | |
| B. | 分子式为CH4O和C2H6O的物质一定互为同系物 | |
| C. | 根据纤维在火焰上燃烧产生的气味,可确定该纤维是否为蛋白纤维 | |
| D. | 等质量的甲醛、葡萄糖、纤维素完全燃烧时的耗氧量相等 |
| A. | 能使润湿的淀粉KI试纸变成蓝色的物质一定是Cl2 | |
| B. | 用硝酸酸化的硝酸银溶液能一次鉴别NaCl,NaBr,KI三种失去标签的溶液 | |
| C. | 某溶液中加入CCl4,CC14层显紫色,证明原溶液中存在I- | |
| D. | 某浅黄色的溴水,加入CC14震荡静置后,上层显橙红色 |
| A. | 常温常压下,11.2L氧气含氧分子数约为3.01×1023个 | |
| B. | 两个体积相同的容器,一个盛有NO,另一个盛有N2和O2的混合气体,在同温同压下两容器内气体分子总数、原子总数和气体质量也一定相等 | |
| C. | 标况下,等质量的O2和O3中所含的氧原子数目相等 | |
| D. | 将98gH2SO4溶于500ml水,得到溶液的物质的量浓度为2.0mol/L |
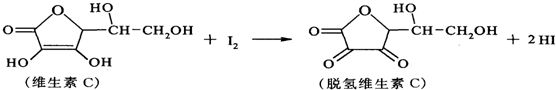
下列说法不正确的是( )
| A. | 上述反应为氧化还原反应 | |
| B. | 维生素C分子中有3种官能团 | |
| C. | 脱氢维生素C不能与氢气发生加成反应 | |
| D. | 脱氢维生素C的分子式为C6H6O6 |
S(s)+2KNO3(s)+3C(s)═K2S(s)+N2(g)+3CO2(g)△H
已知:C(s)+O2(g)═CO2(g)△H1
S(s)+2K(s)═K2S(s)△H2
2K(s)+N2(g)+3O2(g)═2KNO3(s)△H3
则△H为( )
| A. | △H1+△H2-△H3 | B. | △H3+3△H1-△H2 | C. | 3△H1+△H2-△H3 | D. | △H3+△H1-△H2 |
| A. | BaSO4在医学上用作钡餐,Ba2+对人体无毒 | |
| B. | 葡萄糖注射液不能产生丁达尔效应现象,不属于胶体 | |
| C. | ${\;}_{\;}^{14}$C可用于文物年代的鉴定,${\;}_{\;}^{14}$C与${\;}_{\;}^{12}$C互为同素异形体 | |
| D. | 煤的干馏和石油的分馏均属化学变化 |