题目内容
现有碳酸盐矿石(主要成分为CaCO3、BaCO3)需分离出BaCO3,并尽可能除去Ca2+,为完成此分离查得有关溶解度(克/100克水)数据如下:
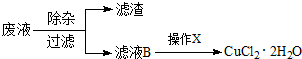
分离要求:(1)原料只有矿石、焦炭、空气和水,不用其它化学原料;(2)Ca2+含量越低越好.如图是分离的实验步骤,在箭头上方注明反应所需条件、方法和所需的物质,在方框里写上各步产物的分子式或化学式.

| 温度 物质 | 0℃ | 50℃ | 80℃ |
| Ca(0H)2 | 0.173 | 0.130 | 0.004 |
| Ba(OH)2 | 1.64 | 13.1 | 101.5 |

考点:物质分离、提纯的实验方案设计,物质的分离、提纯的基本方法选择与应用
专题:实验设计题
分析:由实验目的分离出BaCO3,并尽可能除去Ca2+可知,步骤为矿石高温分解生成CaO、BaO,由表格中的信息可知,加水在80℃溶解,分离出氢氧化钙,然后向氢氧化钡中通入足量的二氧化碳即可,以此来解答.
解答:
解:由实验目的分离出BaCO3,并尽可能除去Ca2+可知,步骤为矿石高温分解生成CaO、BaO,由表格中的信息可知,加水在80℃溶解,分离出氢氧化钙,然后向氢氧化钡中通入足量的二氧化碳即可,则分离的实验步骤如图为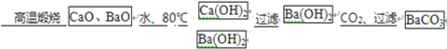 ,
,
故答案为: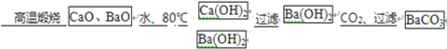 .
.
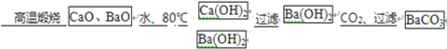 ,
,故答案为:
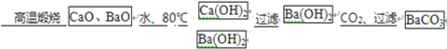 .
.
点评:本题考查混合物的分离提纯的实验方案设计,为高频考点,把握物质的性质及性质差异为解答的关键,侧重分离方法及信息应用能力的考查,题目难度不大.

练习册系列答案
相关题目
下列溶液中微粒浓度关系一定正确的是( )
| A、氨水与氯化铵的pH=7的混合溶液中:c(Cl-)>c(NH4+) |
| B、pH=2的一元酸和pH=12的一元强碱等体积混合:c(OH-)>c(H+) |
| C、0.1mol?L-1的硫酸铵溶液中:c(NH4+)>c(SO42-)>c(H+)>c(OH-) |
| D、0.1mol?L-1的硫化钠溶液中:c(OH-)=c(H+)>c(HS-)>c(H2S) |
一定温度下,向一固定容积的容器中放入1mol A和1mol B,待反应A(s)+B(g)?C(g)+2D(g)达到平衡时,C的体积分数是M%,在相同的条件下,若按以下配比开始反应,平衡时C的体积分数比为M%的是( )
| A、2molA+2molB |
| B、1molD+2molC |
| C、2molD+1molA+1molB |
| D、1molA+0.5molB+0.5molC+1.0molD |

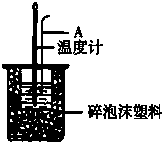 分别取40mL的0.50mol/L盐酸与40mL 0.55mol/L氢氧化钠溶液进行中和反应.通过测定反应过程中所放出的热量可计算中和热.请回答下列问题.
分别取40mL的0.50mol/L盐酸与40mL 0.55mol/L氢氧化钠溶液进行中和反应.通过测定反应过程中所放出的热量可计算中和热.请回答下列问题.