题目内容
19.一定量的混合气体在密闭容器中发生如下反应:mA(g)+nB(g)?pC(g),在一定温度下反应达到平衡,将容器容积缩小到原来的$\frac{1}{2}$,当达到新的平衡时,C的浓度变为原平衡时的1.9倍.若压缩过程中温度恒定,则下列说法中不正确的是( )| A. | m+n<p | B. | 平衡向逆反应方向移动 | ||
| C. | C的体积分数增大 | D. | A的转化率降低 |
分析 mA(g)+nB(g)?pC(g),达到平衡后,温度不变,将气体体积压缩到$\frac{1}{2}$,若平衡不移动,C的浓度为原来的2倍,当达到平衡时C的浓度为原来的1.9倍,则体积减小时平衡逆向移动,以此来解答.
解答 解:mA(g)+nB(g)?pC(g),达到平衡后,温度不变,将气体体积压缩到$\frac{1}{2}$,若平衡不移动,C的浓度为原来的2倍,当达到平衡时C的浓度为原来的1.9倍,则体积减小时平衡逆向移动,
A.体积缩小,相当于加压,平衡逆向移动,则m+n<p,故A正确;
B.由上述分析可知,平衡逆向移动,故B正确;
C.平衡逆向移动,C的体积分数减小,但比原来的大,故C错误;
D.平衡逆向移动,A的转化率降低,故D正确;
故选C.
点评 本题考查影响平衡移动的因素,注意把握“体积压缩到$\frac{1}{2}$,当达到平衡时C的浓度为原来的1.9倍”为解答的关键信息,题目难度中等.

练习册系列答案
相关题目
10.煤化工中常将研究不同温度下的平衡常数,投料比及产率等问题,已知:CO(g)+H2O(g)?H2(g)+CO2(g)的平衡常数随温度的变化如表:下列叙述正确的是( )
| 温度℃ | 400 | 500 | 830 | 1000 |
| 平均常数K | 10 | 9 | 1 | 0.6 |
| A. | 上述反应中正反应是吸热反应 | |
| B. | 该反应的化学平衡常数表达式为K=$\frac{\{c({H}_{2})•c(C{O}_{2})\}}{\{c(CO)•c({H}_{2}O)\}}$ | |
| C. | 该反应在400℃时达平衡状态,若升高温度,则正反应速率减小,逆反应速率增大 | |
| D. | 在830℃,2L的密闭容器中,冲入1molCO、5molH2O(g)、3molCO2和2molH2发生上述反应,在达到平衡前V(正)<V(逆) |
7.在元素周期表中位于金属元素和非金属元素交界处最容易找到的材料是( )
| A. | 制催化剂的材料 | B. | 耐高温、耐腐蚀的合金材料 | ||
| C. | 半导体材料 | D. | 制农药的材料 |
14.下列有关化学用语表示正确的是( )
| A. | 乙烯的结构简式为:C2H4 | |
| B. | S2-的结构示意图: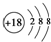 | |
| C. | 质子数为53,中子数为78的碘原子:${\;}_{53}^{131}$I | |
| D. | NH4Cl的电子式为: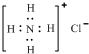 |
4.某溶液中含有SiO32-、Br-、CO32-、Na+,向该溶液中通入过量的Cl2,下列判断不正确的是( )
| A. | SiO32-和Br-浓度都会减小 | B. | 溶液颜色会发生变化 | ||
| C. | 该过程中不会有沉淀生成 | D. | 离子浓度基本保持不变的只有Na+ |
9.工业制备硫酸过程中存在如下反应:2SO2+O2$?_{催化剂}^{450-500℃}$2SO3,下列关于该反应的说法正确的是( )
| A. | 增大O2的浓度能加快反应速率 | B. | 降低体系温度能加快反应速率 | ||
| C. | 使用催化剂不影响反应速率 | D. | 一定条件下SO2能100%转化为SO3 |
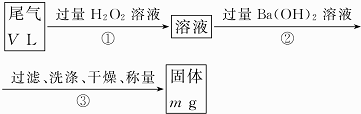
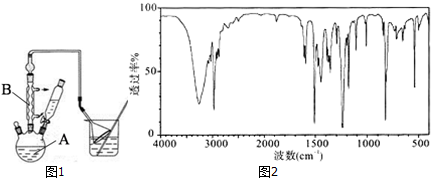
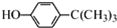 工业用途广泛,可用于生产油溶性酚醛树脂、稳定剂和香料等.实验室以苯酚、叔丁基氯(CH3)3CCl等为原料制备对叔丁基苯酚.实验步骤如下:
工业用途广泛,可用于生产油溶性酚醛树脂、稳定剂和香料等.实验室以苯酚、叔丁基氯(CH3)3CCl等为原料制备对叔丁基苯酚.实验步骤如下: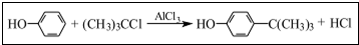 .该反应为放热反应,且实验的产率通常较低,可能的原因是由于叔丁基氯挥发导致产率降低.
.该反应为放热反应,且实验的产率通常较低,可能的原因是由于叔丁基氯挥发导致产率降低.