题目内容
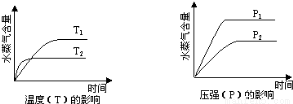
一定条件下,下列反应中水蒸气含量随反应时间的变化趋势符合下图的是
A.CO2(g)+2NH3(g) CO(NH2)2(s)+H2O(g) ΔH<0
CO(NH2)2(s)+H2O(g) ΔH<0
B.CO2(g)+H2(g) CO(g)+H2O(g) ΔH>0
CO(g)+H2O(g) ΔH>0
C.CH3CH2OH(g) CH2==CH2(g)+H2O(g) ΔH>0
CH2==CH2(g)+H2O(g) ΔH>0
D.2C6H5CH2CH3(g)+O2(g) 2C6H5CH==CH2(g)+2H2O(g) ΔH<0
2C6H5CH==CH2(g)+2H2O(g) ΔH<0
A
【解析】
试题分析:温度越高,反应越快,到达平衡的时间就越少,因此t2>t1;同理压强越大,反应越快,到达平衡的时间就越少,因此p1>p2;A、反应是一个体积减小的、放热的可逆反应,因此升高温度平衡向逆反应方向移动,降低水蒸气的含量;而增大压强平衡向正反应方向移动,增大水蒸气的含量,A正确;B、反应是一个体积不变的、吸热的可逆反应,压强对水蒸气的含量不影响;升高温度平衡向正反应方向移动,增大水蒸气的含量,因此均不符合,B错误;C、反应是一个体积增大的、吸热的可逆反应,升高温度平衡向正反应方向移动,增大水蒸气的含量,不符合图象,C错误;D、反应是一个体积增大的、放热的可逆反应,压强不符合,D错误.答案选A。
考点:考查化学平衡的影响因素及图表。

T1温度下,反应2SO2(g)+O2(g)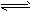 2SO3(g) △H<0的平衡常数K=532.4。
2SO3(g) △H<0的平衡常数K=532.4。
(1)该反应平衡常数的表达式为K= ,T1温度下,某时刻测得体系中各物质浓度分别为c(SO2)=0.0600 mol·L-1,c(O2)=0.400 mol·L-1,c(SO3)=2.000mol·L-1,此时反应进行的方向为 。
(2)该反应△S 0,升高温度,平衡常数 (填“增大”“减小”或“不变”)
(3)T2温度下,2L容积固定的甲、乙两密闭容器中发生上述反应,测得平衡时有关数据如下:
容器 | 甲 | 乙 |
反应物投入量 | 2molSO2、1molO2 | 4molSO3 |
平衡时n(SO3)/mol | 1 | m |
反应物的转化率 | ?1 | ?2 |
①下列能说明T2温度下甲容器中上述反应已达到平衡状态的是 。
A.SO2、O2、SO3的物质的量浓度之比为2:1:2
B.容器内气体压强不再变化
C.单位时间内2v(SO2)消耗= v(O2)生成
D.容器内混合气体的密度不再变化
②分析表格中数据,?1+?2 1(填“>”“=”或“<”),T1 T2(填“>”“=”或“<”)。
(14分)2013年10月9日,2013年诺贝尔化学奖在瑞典揭晓,犹太裔美国理论化学家马丁·卡普拉斯、美国斯坦福大学生物物理学家迈克尔·莱维特和南加州大学化学家亚利耶·瓦谢尔因给复杂化学体系设计了多尺度模型而分享奖项。三位科学家的研究成果已经应用于废气净化及植物的光合作用的研究中,并可用于优化汽车催化剂、药物和太阳能电池的设计。
(1)汽车尾气净化的主要原理为:2NO(g) + 2CO(g) 2CO2(g)+ N2(g) △H<0同一条件下该反应正反应的平衡常数为K1,逆反应的表达式平衡常数为K2,K1与K2的关系式为 。
2CO2(g)+ N2(g) △H<0同一条件下该反应正反应的平衡常数为K1,逆反应的表达式平衡常数为K2,K1与K2的关系式为 。
(2)若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是 (填代号)。
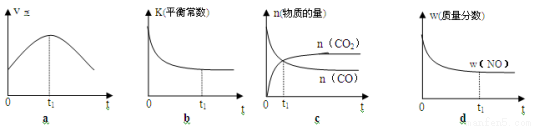
(3)在体积为10L的密闭容器中,加入一定量的CO2和H2,在900℃时发生吸热反应并记录前5min各物质的浓度,第6min改变了条件。各物质的浓度变化如下表;
时间/min | CO2(mol·L-1) | H2(mol·L-1) | CO(mol·L-1) | H2O(mol·L-1) |
0 | 0.2000 | 0.3000 | 0 | 0 |
2 | 0.1740 | 0.2740 | 0.0260 | 0.0260 |
5 | 0.0727 | 0.1727 | 0.1273 | 0.1273 |
6 | 0.0350 | 0.1350 | 0.1650 |
①前2min,用CO表示的该化学反应的速率为 ;
②第5—6min,平衡移动的可能原因是 ;
(4)直接排放煤燃烧产生的烟气会引起严重的环境问题。煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
已知:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867 kJ·mol-1
2NO2(g)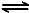 N2O4(g) △H=-56.9 kJ·mol-1
N2O4(g) △H=-56.9 kJ·mol-1
H2O(g) = H2O(l) △H = -44.0 kJ·mol-1
写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式: 。
在一定条件下,可以用NH3处理NOx。已知NO与NH3发生反应生成N2和H2O,现有NO和NH3的混合物1mol,充分反应后得到的还原产物比氧化产物多1.4 g,则原反应混合物中NO的物质的量可能是 mol
(6)在一定条件下,也可以用H2处理CO合成甲醇和二甲醚(CH3OCH3)及许多烃类物质。当两者以物质的量1:1催化反应,其原子利用率达100%,合成的物质可能是 。
a.汽油 b.甲醇 c.甲醛 d.乙酸
反应C(s)+H2O(g) CO(g)+H2(g)在一可变容积的密闭容器内进行,达到平衡后,保持其他条件不变,下列条件的改变一定能使平衡移动的是
CO(g)+H2(g)在一可变容积的密闭容器内进行,达到平衡后,保持其他条件不变,下列条件的改变一定能使平衡移动的是
A.增加C的质量
B.保持体积不变,充入氦气使体系压强增大
C.加入催化剂
D.保持压强不变,充入氦气使容器体积增大
物质 | X | Y | Z |
初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
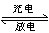 LiCoO2+6C,下列说法错误的是
LiCoO2+6C,下列说法错误的是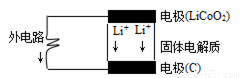
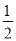 O2(g)===CO(g) ΔH2
O2(g)===CO(g) ΔH2