题目内容
14.三氯化硼的熔点为-107℃,沸点为12.5℃,在其分子中键与键之间的夹角为120°,它能水解,有关叙述正确的是( )| A. | 氯化硼液态时能导电而固态时不导电 | |
| B. | 硼原子以sp3杂化 | |
| C. | 氯化硼分子属极性分子 | |
| D. | 氯化硼遇水蒸气会产生白雾 |
分析 A.氯化硼是共价化合物;
B.三氯化硼中的硼为sp2杂化;
C.正负电荷重心重合的分子是非极性分子,正负电荷重心不重合的是极性分子;
D.三氯化硼水解生成HCl,氯化氢极易溶于水.
解答 解:A.氯化硼是共价化合物液态时不能导电,故A错误;
B.三氯化硼中硼原子含有3个σ键且不含孤电子对,采用sp2杂化,故B错误;
C.三氯化硼中的硼为sp2杂化,无孤对电子,分子中键与键之间的夹角为120°,是平面三角形结构,该分子正负电荷重心重合,所以是非极性分子,故C错误;
D.三氯化硼水解生成的HCl在空气中形成白雾,故D正确.
故选D.
点评 本题考查原子轨道杂化,分子极性等,难度适中,注意三氯化硼中的硼为sp2杂化,无孤对电子,分子中键与键之间的夹角为120°,是平面三角形结构,属非极性分子.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.在体积为2L的恒容密闭容器中发生反应xA(g)+yB(g)═zC(g),图I表示200℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系.则下列结论正确的是( )
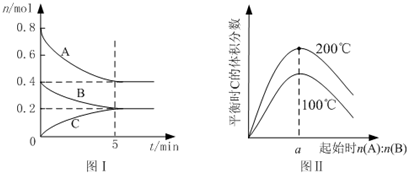

| A. | 200℃时,反应从开始到平衡的平均速率v(B)=0.04mol•L-1•min-1 | |
| B. | 图Ⅱ所知反应xA(g)+yB(g)?zC(g)+Q(Q>0) | |
| C. | 若在图Ⅰ所示的平衡状态下,再向体系中充入He,重新达到平衡前v(正)>v(逆) | |
| D. | 由图I可知,该反应式为2A(g)+B(g)?C(g) |
5.下列各组离子,能在溶液中大量共存的是( )
| A. | K+、H+、SO42-、OH- | B. | Na+、H+、Cl-、SO42- | ||
| C. | Na+、Ca2+、CO32-、NO3- | D. | Ba2+、Cu2+、Cl-、SO42- |
2.下列说法中正确的为( )
| A. | 原子得失电子能力与该原子最外层电子数多少有关 | |
| B. | ⅠA族、ⅡA族元素的阳离子与同周期稀有气体元素的原子具有相同的核外电子排布 | |
| C. | ⅦA族元素的原子随核电荷数的增加,得电子能力逐渐减弱 | |
| D. | 前三周期元素中共有非金属元素12种 |
19.SO2通入足量Fe(NO3)3稀溶液中,溶液由棕色变为浅绿色,但立即又变为棕黄色,这时若滴入BaCl2溶液,会产生白色沉淀.针对上述一系列变化过程中,下列说法中不正确的是( )
| A. | 上述过程中,最终被还原的是NO3- | |
| B. | 从上述过程中可以得出结论,氧化性:HNO3>Fe3+>稀H2SO4 | |
| C. | 假设通入的SO2完全反应,则同温同压下,SO2和逸出气体的体积为1:1 | |
| D. | 上述过程中,会产生一种无色的难溶于水的气体 |
4.用NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A. | 1mol铁与足量的氯气完全反应转移的电子数为2NA | |
| B. | 常温常压下,11.2L氯化氢气体中含有的分子数为0.5NA | |
| C. | 标准状况下,1molCO2、CO的混合气中含有的碳原子数为NA | |
| D. | 1L1mol•L-1CuCl2溶液中含有的氯离子数为NA |
 .预测该芳香烃能(填“能”或“不能”)发生该类反应.
.预测该芳香烃能(填“能”或“不能”)发生该类反应.
 c.
c.