题目内容
|
离子晶体不可能具有的性质是 | |
| [ ] | |
A. |
较高的熔、沸点 |
B. |
良好的导电性 |
C. |
溶于极性溶剂 |
D. |
坚硬而易粉碎 |
解析:
|
解析:离子晶体是阴、阳离子通过离子键结合而成的,在固态时,阴、阳离子受到彼此的束缚不能自由移动,因而不导电.只有在溶于水或熔融后,电离成可以自由移动的阴、阳离子,才能导电. 知识归纳:离子晶体的性质:①硬度较大,难于压缩;②熔沸点较高;③固体不导电;④延展性差,受到外力容易破碎.⑤部分离子化合物易溶于水. |

 53随堂测系列答案
53随堂测系列答案下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
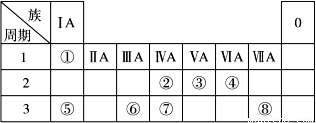
(1)地壳中含量居于第二位的元素在周期表中的位置是________________。
(2)②的最高价氧化物固态时的晶体类型:______________;⑦的最高价氧化物固态时的晶体类型:______________。
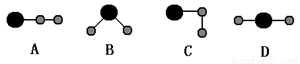
(3)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式______________,______________。若用球棍模型表示①和④形成的化合物的分子结构,应该是_____________。
(4)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是( )
A.最高正化合价为+6价, B.气态氢化物比H2S稳定,
C.最高价氧化物的水化物的酸性比硫酸弱, D.单质在常温下可与氢气化合。
(5) 已知X为ⅡA族元素(第一到第七周期),其原子序数为a,Y与X位于同一周期,且为ⅢA族元素,则Y的原子序数b与a所有可能的关系式___________________________。
(6)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
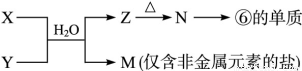
X溶液与Y溶液反应的离子方程式________, M中阳离子的鉴定方法____________。