题目内容
下列装置或操作能达到实验目的是( )


| A、①防止铁钉生锈 |
| B、②构成铜锌原电池 |
| C、③中和热测定 |
| D、④验证NaCl溶液(含酚酞)电解产物 |
考点:化学实验方案的评价
专题:
分析:A.作原电池负极或电解池阳极的金属加速被腐蚀;
B.含有盐桥的原电池中,金属电极材料和电解质溶液中金属元素属于同一种元素;
C.中和热的测定中需要环形玻璃棒搅拌;
D.电解氯化钠溶液时,阳极上生成氯气、阴极上生成氢气,且阴极附近生成NaOH,氯气能使湿润的淀粉碘化钾试纸变蓝色,酚酞试液遇碱变红色.
B.含有盐桥的原电池中,金属电极材料和电解质溶液中金属元素属于同一种元素;
C.中和热的测定中需要环形玻璃棒搅拌;
D.电解氯化钠溶液时,阳极上生成氯气、阴极上生成氢气,且阴极附近生成NaOH,氯气能使湿润的淀粉碘化钾试纸变蓝色,酚酞试液遇碱变红色.
解答:
解:A.作原电池负极或电解池阳极的金属加速被腐蚀,该装置中铁钉作阳极,加速被腐蚀,所以不能防止铁生锈,故A错误;
B.含有盐桥的原电池中,金属电极材料和电解质溶液中金属元素属于同一种元素,所以应该将铜插入硫酸铜溶液中、锌插入硫酸锌溶液中才能构成原电池,故B错误;
C.中和热的测定中需要环形玻璃棒搅拌,否则温度不均匀,导致测量不准确,故C错误;
D.电解氯化钠溶液时,阳极上生成氯气、阴极上生成氢气,且阴极附近生成NaOH,氯气能使湿润的淀粉碘化钾试纸变蓝色,酚酞试液遇碱变红色,所以该装置能实现实验目的,故D正确;
故选D.
B.含有盐桥的原电池中,金属电极材料和电解质溶液中金属元素属于同一种元素,所以应该将铜插入硫酸铜溶液中、锌插入硫酸锌溶液中才能构成原电池,故B错误;
C.中和热的测定中需要环形玻璃棒搅拌,否则温度不均匀,导致测量不准确,故C错误;
D.电解氯化钠溶液时,阳极上生成氯气、阴极上生成氢气,且阴极附近生成NaOH,氯气能使湿润的淀粉碘化钾试纸变蓝色,酚酞试液遇碱变红色,所以该装置能实现实验目的,故D正确;
故选D.
点评:本题考查实验方案评价,为高考高频点,涉及金属腐蚀与防护、原电池原理、中和热测定、电解原理等知识点,侧重实验操作和实验原理的考查,注意实验方案的操作性、可行性、评价性分析,题目难度不大.

练习册系列答案
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案
相关题目
下列各对物质能发生离子反应的是( )
| A、AgNO3,KClO3 |
| B、Na2CO3,H2SO4 |
| C、Cu,盐酸 |
| D、Na2CO3,K2SO4 |
容量瓶常见的规格有( )
| A、50mL |
| B、100mL |
| C、180mL |
| D、1000mL |
NaOH、Na2CO3、NaCl、Na2SO4可按某种标准划为一类物质,下列分类标准不正确的是( )
| A、可与硝酸反应 | B、钠的化合物 |
| C、可溶于水 | D、电解质 |



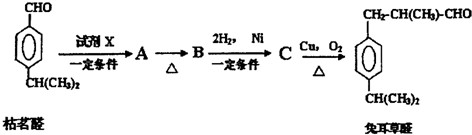
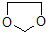 在酸性条件下生成氯吡格雷和另一种常见有机物,该有机物在浓硫酸催化下,加热脱水生成乙炔,试写出该有机物脱水生成乙炔的方程式
在酸性条件下生成氯吡格雷和另一种常见有机物,该有机物在浓硫酸催化下,加热脱水生成乙炔,试写出该有机物脱水生成乙炔的方程式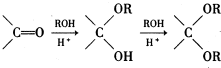
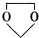 的合成路线流程图(无机试剂任选).合成路线流程示意图为:
的合成路线流程图(无机试剂任选).合成路线流程示意图为: