题目内容
15.A、B、C为短周期元素,在周期表中所处的位置如图所示,A、C两元素的原子核外电子数之和等于B原子的质子数,B原子核内质子数和中子数相等.| A | C | |
| B |
(2)B元素最高价氧化物对应水化物的化学式为H2SO4,该化合物为共价(填“共价”或“离子”)化合物.
(3)C的原子结构示意图为
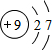 ,C的单质与H2反应的化学方程式为:H2+F2=2HF
,C的单质与H2反应的化学方程式为:H2+F2=2HF(4)由元素A、C及氢元素形成的化合物中含有的化学键的类型有离子键、共价键.
分析 由A、B、C为短周期元素,结合在周期表中所处的位置可知,A、C为第二周期元素,设A的质子数为x,C的质子数为x+2,B的质子数为x+9,A、C两元素的原子核外电子数之和等于B原子的质子数,则x+x+2=x+9,解得x=7,即A为N,C为F,B原子核内质子数和中子数相等,B为S,然后结合元素化合物知识来解答.
解答 解:由A、B、C为短周期元素,结合在周期表中所处的位置可知,A、C为第二周期元素,设A的质子数为x,C的质子数为x+2,B的质子数为x+9,A、C两元素的原子核外电子数之和等于B原子的质子数,则x+x+2=x+9,解得x=7,即A为N,C为F,B原子核内质子数和中子数相等,B为S,
(1)A、C元素的名称分别为氮、氟,故答案为:氮;氟;
(2)B元素最高价氧化物对应水化物的化学式为H2SO4,只含共价键,该化合物为共价化合物,故答案为:H2SO4;共价;
(3)C的原子结构示意图为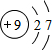 ,C的单质与H2反应的化学方程式为H2+F2=2HF,故答案为:
,C的单质与H2反应的化学方程式为H2+F2=2HF,故答案为: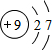 ;H2+F2=2HF;
;H2+F2=2HF;
(4)由元素A、C及氢元素形成的化合物为NH4F,含有的化学键的类型有离子键、共价键,故答案为:离子键、共价键.
点评 本题考查位置、结构与性质的应用,为高频考点,把握元素的位置、原子结构推断元素为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
相关题目
15.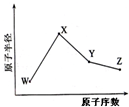 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图.已知W的一种核素的质量数为18,中子数为10,X原子和Ne原子的核外电子数相差1,Y的单质是一种常见的半导体材料,Z的非金属性在同周期元素中最强.下列说法错误的是( )
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图.已知W的一种核素的质量数为18,中子数为10,X原子和Ne原子的核外电子数相差1,Y的单质是一种常见的半导体材料,Z的非金属性在同周期元素中最强.下列说法错误的是( )
 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图.已知W的一种核素的质量数为18,中子数为10,X原子和Ne原子的核外电子数相差1,Y的单质是一种常见的半导体材料,Z的非金属性在同周期元素中最强.下列说法错误的是( )
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图.已知W的一种核素的质量数为18,中子数为10,X原子和Ne原子的核外电子数相差1,Y的单质是一种常见的半导体材料,Z的非金属性在同周期元素中最强.下列说法错误的是( )| A. | 对应简单离子半径X<W | |
| B. | 对应气态氢化物的稳定性Y<Z | |
| C. | 化合物XZW既含离子键又含共价键 | |
| D. | Z或X的最高价氧化物对应的水化物均能与Y的氧化物反应 |
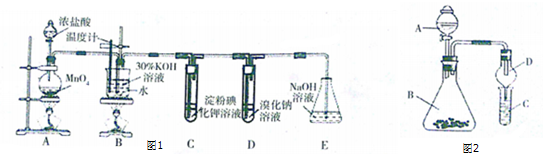
6.影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究.
实验一:甲同学研究的实验报告如表:
该同学的实验目的是研究物质本身的性质对反应速率的影响;根据控制变量法,要得出正确的实验结论,还需控制的实验条件是保持温度相同.
实验二:已知2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+8H2O+10CO2↑,在高锰酸钾酸性溶液和草酸溶液反应时,发现开始一段时间反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快.
(1)针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快.从影响化学反应速率的因素看,你猜想反应速率明显加快的原因还可能是生成的锰离子有催化作用.
(2)若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液外,还需要选择的试剂最合理的是B(选填编号).
A.硫酸钾 B.硫酸锰 C.水 D.氯化锰.
实验一:甲同学研究的实验报告如表:
| 实 验 步 骤 | 现 象 | 结 论 |
| ①分别取等体积的2mol/L硫酸于试管中; ②分别投入大小、形状相同的Cu、Fe、Mg. | 反应快慢: Mg>Fe>Cu | 反应物的性质越活泼,反应速率越快. |
实验二:已知2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+8H2O+10CO2↑,在高锰酸钾酸性溶液和草酸溶液反应时,发现开始一段时间反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快.
(1)针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快.从影响化学反应速率的因素看,你猜想反应速率明显加快的原因还可能是生成的锰离子有催化作用.
(2)若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液外,还需要选择的试剂最合理的是B(选填编号).
A.硫酸钾 B.硫酸锰 C.水 D.氯化锰.
3.某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.
(1)催化剂能加快化学反应速率的原因是降低了活化能.
(2)常温下5% H2O2溶液的pH约为6,H2O2的电离方程式为⇒H2O2?H++HO2-.
(3)实验①和②的目的是探究浓度对反应速率的影响.
(4)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图.
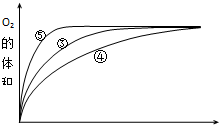
分析上图能够得出的实验结论是碱性环境能增大H2O2分解的速率,酸性环境能减小H2O2分解的速率.
| 实验编号 | 反应物 | 催化剂 |
| ① | 10mL2% H2O2溶液 | 无 |
| ② | 10mL5% H2O2溶液 | 无 |
| ③ | 10mL5% H2O2溶液 | 1mL0.1mol•L-1FeCl3溶液 |
| ④ | 10mL5% H2O2溶液+少量HCl溶液 | 1mL0.1mol•L-1FeCl3溶液 |
| ⑤ | 10mL5% H2O2溶液+少量NaOH溶液 | 1mL0.1mol•L-1FeCl3溶液 |
(2)常温下5% H2O2溶液的pH约为6,H2O2的电离方程式为⇒H2O2?H++HO2-.
(3)实验①和②的目的是探究浓度对反应速率的影响.
(4)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图.

分析上图能够得出的实验结论是碱性环境能增大H2O2分解的速率,酸性环境能减小H2O2分解的速率.
10.X、Y、Z三种非金属元素具有相同的电子层数,它们的气态氢化物的稳定性的强弱顺序为XH3<H2Y<HZ,下列说法中正确的是( )
| A. | 原子序数:X>Y>Z | B. | 非金属性:X<Y<Z | ||
| C. | 原子半径:X<Y<Z | D. | 原子得电子能力:X>Y>Z |
20.下列各组的电极材料和电解液,不能组成原电池的是( )
| A. | 铜片、石墨棒,乙醇 | B. | 铜片、石墨棒,硝酸银溶液 | ||
| C. | 锌片、铜片,稀盐酸 | D. | 铜片、铂片,FeCl3溶液 |
4.下列有关化学用语表示正确的是( )
| A. | 质子数和中子数均为6的碳原子:${\;}_{6}^{6}$C | |
| B. | 硫离子的结构示意图: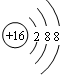 | |
| C. | 氢氧化钠的电子式: | |
| D. | 氮气分子的电子式: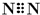 , , |
5.有一种有机物C4H4其分子结构如图所示,有关该分子说法正确的是( )
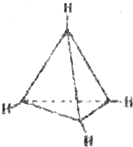

| A. | 该分子是极性分子 | B. | 每个碳原子均为sp2杂化 | ||
| C. | 分子中有极性键和非极性键 | D. | 分子中共有4个碳碳键 |