题目内容
10.常温下,下列物质能用铝制器皿盛放的是( )| A. | 稀硫酸 | B. | 氢氧化钠溶液 | C. | 稀硝酸 | D. | 浓硝酸 |
分析 Al与酸、强碱均发生反应,但常温下Al遇浓硝酸或浓硫酸发生钝化,以此来解答.
解答 解:A.稀硫酸有弱氧化性,能和铝反应生成氢气,不能用铝制品容器盛放,故A错误;
B.氢氧化钠溶液能和铝反应生成氢气,不能用铝制品容器盛放,故B错误;
C.铝与稀硝酸溶液发生氧化还原反应,不能用铝制品容器盛放,故C错误;
D.浓硝酸是强氧化性的酸,铝在浓硝酸中发生钝化现象,故铝制品容器可以盛放浓硝酸,故D正确;
故选D
点评 本题考查Al的性质,为高频考点,把握物质的性质、性质与用途为解答的关键,侧重分析与应用能力的考查,注意钝化生成致密的氧化膜阻止反应的进一步发生,题目难度不大.

练习册系列答案
相关题目
20.根据图,下列判断中正确的是( )
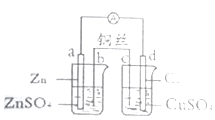

| A. | 电路中电子的流动方向:a-d-CuSO4(aq)一c一b | |
| B. | 该原电池原理:Zn+CuSO4═ZnSO4+Cu | |
| C. | c电极质量减少量等于d电极质量增加量 | |
| D. | d电极反应:Cu2++2e-=Cu,反应后CuSO4溶液浓度下降 |
1.设NA为阿伏加德罗常数.下列说法中正确的是( )
| A. | 14gC8H16中的共用电子对数为3NA | |
| B. | 1mol苯中的碳碳双键数目为3NA | |
| C. | 1mol 二肽中含有的肽键数目为2NA | |
| D. | 30g甲酸甲酯与甲醛的混合物完全燃烧,生成的CO2的分子数为1.5NA |
18.下列元素中,最高正化合价数值最大的是( )
| A. | C | B. | F | C. | S | D. | Na |
5.仅用下表中提供的玻璃仪器(非玻璃仪器任选)不能实现相应实验目的是( )
| 选项 | 实验目的 | 玻璃仪器 |
| A | 配制一定质量分数的NaCl溶液 | 胶头滴管、量筒、烧杯、玻璃棒 |
| B | 测定NaOH溶液浓度 | 滴定管、锥形瓶、烧杯 |
| C | 鉴别葡萄糖和蔗糖 | 试管、烧杯、酒精灯 |
| D | 实验室用浓氨水和生石灰制备氨气 | 长颈漏斗、烧杯、玻璃棒 |
| A. | A | B. | B | C. | C | D. | D |
15.乙烯是重要的工业原料,下列有关乙烯叙述不正确的是 ( )
| A. | 常温常压下是气体 | B. | 能使溴的四氯化碳溶液褪色 | ||
| C. | 不能使酸性高锰酸钾溶液褪色 | D. | 在一定条件下能够聚合生成聚乙烯 |
2.在实验室中,下列各图所示操作能达到对应实验目的是( )
| A. |  分离乙酸和乙醇 | B. |  制取少量蒸馏水 | ||
| C. |  转移溶液 | D. |  分离碘和酒精 |
19.以溴乙烷为原料制备1,2─二溴乙烷(反应条件略去),方案中最合理的是( )
| A. | CH3CH2Br→CH3CH2OH→CH2=CH2$\stackrel{Br_{2}}{→}$CH2BrCH2Br | |
| B. | CH3CH2Br$\stackrel{Br_{2}}{→}$CH2BrCH2Br | |
| C. | CH3CH2Br→CH2=CH2 $\stackrel{HBr}{→}$CH2BrCH3$\stackrel{Br_{2}}{→}$CH2BrCH2Br | |
| D. | CH3CH2Br→CH2=CH2 $\stackrel{Br_{2}}{→}$CH2BrCH2Br |
 氮的重要化合物,如氨(NH3)、肼(N2H4)、三氟化氮(NF3)等在生产、生活中具有重要作用.
氮的重要化合物,如氨(NH3)、肼(N2H4)、三氟化氮(NF3)等在生产、生活中具有重要作用.