题目内容
设NA为阿伏加德罗常数,下列说法正确的是( )
| A、标准状况下,1mol H2O的体积约为22.4L |
| B、1 L 1mol/L Na2CO3溶液中Na+的物质的量为1mol |
| C、NA个氢气分子所占的体积为22.4L |
| D、常温常压下NA个二氧化碳分子的质量为44g |
考点:阿伏加德罗常数
专题:
分析:A.标准状况下,水的状态不是气体,不能使用标况下的气体摩尔体积计算水的体积;
B.根据碳酸钠的化学式可知,1mol碳酸钠中含有2mol钠离子;
C.没有告诉在标况下,不能使用标况下的气体摩尔体积计算氢气的体积;
D.NA个二氧化碳分子的物质的量为1mol,1mol二氧化碳的质量为44g.
B.根据碳酸钠的化学式可知,1mol碳酸钠中含有2mol钠离子;
C.没有告诉在标况下,不能使用标况下的气体摩尔体积计算氢气的体积;
D.NA个二氧化碳分子的物质的量为1mol,1mol二氧化碳的质量为44g.
解答:
解:A.标况下水不是气体,不能使用标况下的气体摩尔体积计算1mol水的体积,故A错误;
B.1 L 1mol/L Na2CO3溶液中含有溶质碳酸钠1mol,1mol碳酸钠含有2mol钠离子,故B错误;
C.不是标况下,题中条件无法计算氢气的体积,故C错误;
D.NA个二氧化碳分子的物质的量为1mol,其质量为:44g/mol×1mol=44g,故D正确;
故选D.
B.1 L 1mol/L Na2CO3溶液中含有溶质碳酸钠1mol,1mol碳酸钠含有2mol钠离子,故B错误;
C.不是标况下,题中条件无法计算氢气的体积,故C错误;
D.NA个二氧化碳分子的物质的量为1mol,其质量为:44g/mol×1mol=44g,故D正确;
故选D.
点评:本题考查阿伏加德罗常数的有关计算和判断,侧重考查标况下气体摩尔体积的使用条件,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确标况下气体摩尔体积的使用条件为解答关键,试题有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力

练习册系列答案
相关题目
能将(NH4)2SO4、K2SO4、NH4Cl、KCl四种溶液鉴别开的试剂是( )
| A、NaOH溶液 |
| B、Ba(OH)2溶液 |
| C、BaCl2溶液 |
| D、AgNO3溶液 |
能证明醋酸是一种弱酸的事实是( )
| A、醋酸溶液能跟钠反应放出H2 |
| B、1mol/L醋酸溶液的pH小于7 |
| C、1mol/L醋酸钠溶液的pH约为9 |
| D、醋酸钠跟硫酸反应生成醋酸 |
反应aA(g)+bB(g)?cC(g)△H,生成物C的质量分数与压强P和温度T的关系如图,方程式中的系数和△H的大小符合图象的是( )
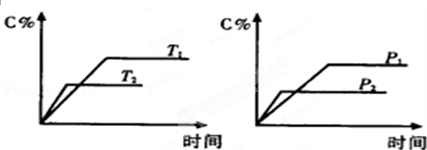

| A、a+b=c△H>0 |
| B、a+b>c△H<0 |
| C、a+b<c△H>0 |
| D、a+b<c△H<0 |
下列说法不符合IA族元素性质特征的是( )
| A、易形成+1价离子 |
| B、从上到下熔沸点逐渐升高 |
| C、从上到下原子半径逐渐增大 |
| D、从上到下金属性依次增强 |
下列应用化学学科研究物质性质的基本方法或所得结论中,不正确的是( )
| A、根据物质的元素组成,将纯净物分为单质和化合物 |
| B、通过镁、锌、铁分别与稀盐酸反应的实验现象,比较不同金属的活泼性强弱 |
| C、根据铁制品表面的锈可用稀盐酸溶解除去的事实,说明铁锈主要成分是酸性氧化物 |
| D、打开盛装浓盐酸的试剂瓶塞,观察现象,了解盐酸的某些物理性质 |