题目内容
1.在标准状况下,将28L HCl气体溶液在水中配成250mL盐酸溶液(1)求所得盐酸的物质的量浓度5mol/L
(2)若取此溶液50mL再稀释成1L溶液,求稀释后盐酸的物质的量浓度0.25mol/L.
分析 依据n=$\frac{V}{Vm}$计算气体的物质的量,依据c=$\frac{n}{V}$计算溶液的物质的量浓度;
依据溶液稀释过程中溶质的物质的量不变计算稀释后盐酸的物质的量浓度.
解答 解:(1)标准状况下,将28L HCl气体物质的量为:$\frac{28L}{22.4L/mol}$=1.25mol,盐酸的物质的量浓度为:$\frac{1.25mol}{0.25L}$=5mol/L;
故答案为:5mol/L;
(2)设稀释后盐酸物质的量浓度为c′则依据溶液稀释过程中溶质的物质的量不变计算得:5mol/L×50mL=1000mL×c′,解得c′=0.25mol/L;
故答案为:0.25mol/L.
点评 本题考查了物质的量浓度有个计算,明确以物质的量为核心计算公式、熟悉溶液稀释规律是解题关键,题目难度不大.

练习册系列答案
相关题目
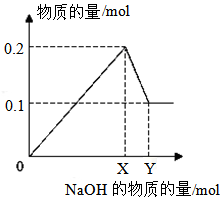
16.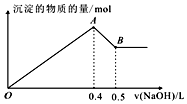 现有AlCl3和MgSO4混合溶液,向其中不断加入NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示,原溶液中Cl-与SO42-的物质的量之比为( )
现有AlCl3和MgSO4混合溶液,向其中不断加入NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示,原溶液中Cl-与SO42-的物质的量之比为( )
 现有AlCl3和MgSO4混合溶液,向其中不断加入NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示,原溶液中Cl-与SO42-的物质的量之比为( )
现有AlCl3和MgSO4混合溶液,向其中不断加入NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示,原溶液中Cl-与SO42-的物质的量之比为( )| A. | 1:3 | B. | 3:1 | C. | 2:3 | D. | 6:1 |
6.下列有关化学用语表示不正确的是( )
| A. | F-的结构示意图: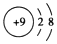 | |
| B. | 中子数为20的氯原子:${\;}_{17}^{20}$Cl | |
| C. | S2-的结构示意图: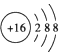 | |
| D. | 原子核内有18个中子的氯原子:${\;}_{17}^{35}$Cl |
11. 当前情况下散烧煤和没有清洁的煤是造成中国城市雾霾或者东部雾霾的主要原因,煤的气化是解决雾霾,清洁地利用煤炭的重要途径之一.
当前情况下散烧煤和没有清洁的煤是造成中国城市雾霾或者东部雾霾的主要原因,煤的气化是解决雾霾,清洁地利用煤炭的重要途径之一.
(1)已知:H2O(g)=H2O(l)△H=44KJ/mol
①请写出煤的气化反应生成合成气(CO和H2)的热化学方程式H2O(g)+C(s)=CO(g)+H2(g)△H=+131.3kJ/mol.
②在恒温、恒容的反应器中,能表明上述反应达到平衡状态的是abef.
a.混合气体平均相对分子质量不再改变 b.气体压强不再改变
c.各气体浓度相等 d.反应体系中温度保持不变
e.断裂氢氧键速率是断裂氢氢键速率的2倍 f.混合提前密度不变
g.单位时间内,消耗水的质量与生成氢气的质量比为9:1
(2)甲醇是重要的化工原料,又可作为燃料,工业上利用合成气(主要成分为CO、CO2、H2)在催化剂的作用下合成甲醇,其中部分主要反应如下:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-58kJ/mol
①请推断该反应自发进行的条件为由于该反应△S<0,△H<0,故根据△G=△H-T△S<0,反应自发,可判断该反应在低温下能自发进行.
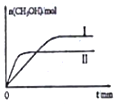
②若将1 mol CO2和2 mol H2充入容积为2L的恒容密闭容器中,在两种不同温度下发生反应,测得CH3OH的物质的量随时间的变化如图所示.曲线Ⅰ、Ⅱ对应的平成常数大小关系为KⅠ>KⅡ(填“>”或“=”或“<”);若5 min后反应达到平衡状态,H2的转化率为90%,则用CO2表示的平均反应速率为0.06mol/(L.min),该温度下的平衡常数为450;若容器容积不变,下列措施可增加甲醇产率的是d.
a.升高温度 b.使用合适的催化剂 c.充入He d.按原比例再充入CO2和H2
③CH4燃料电池利用率很高,装置中添加1L 2mol/L的KOH溶液为电解质,持续缓慢通入标准状况下甲烷2.24L时负极电极反应为CH4-8e-+10OH-=CO32-+7H2O.
 当前情况下散烧煤和没有清洁的煤是造成中国城市雾霾或者东部雾霾的主要原因,煤的气化是解决雾霾,清洁地利用煤炭的重要途径之一.
当前情况下散烧煤和没有清洁的煤是造成中国城市雾霾或者东部雾霾的主要原因,煤的气化是解决雾霾,清洁地利用煤炭的重要途径之一.(1)已知:H2O(g)=H2O(l)△H=44KJ/mol
| 物质 | H2(g) | C(s) | CO(g) |
| 燃烧热KJ/mol | 285.8 | 393.5 | 283.0 |
②在恒温、恒容的反应器中,能表明上述反应达到平衡状态的是abef.
a.混合气体平均相对分子质量不再改变 b.气体压强不再改变
c.各气体浓度相等 d.反应体系中温度保持不变
e.断裂氢氧键速率是断裂氢氢键速率的2倍 f.混合提前密度不变
g.单位时间内,消耗水的质量与生成氢气的质量比为9:1
(2)甲醇是重要的化工原料,又可作为燃料,工业上利用合成气(主要成分为CO、CO2、H2)在催化剂的作用下合成甲醇,其中部分主要反应如下:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-58kJ/mol
①请推断该反应自发进行的条件为由于该反应△S<0,△H<0,故根据△G=△H-T△S<0,反应自发,可判断该反应在低温下能自发进行.
②若将1 mol CO2和2 mol H2充入容积为2L的恒容密闭容器中,在两种不同温度下发生反应,测得CH3OH的物质的量随时间的变化如图所示.曲线Ⅰ、Ⅱ对应的平成常数大小关系为KⅠ>KⅡ(填“>”或“=”或“<”);若5 min后反应达到平衡状态,H2的转化率为90%,则用CO2表示的平均反应速率为0.06mol/(L.min),该温度下的平衡常数为450;若容器容积不变,下列措施可增加甲醇产率的是d.
a.升高温度 b.使用合适的催化剂 c.充入He d.按原比例再充入CO2和H2
③CH4燃料电池利用率很高,装置中添加1L 2mol/L的KOH溶液为电解质,持续缓慢通入标准状况下甲烷2.24L时负极电极反应为CH4-8e-+10OH-=CO32-+7H2O.
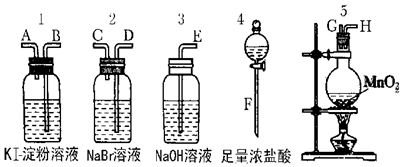
 I.20mL0.1mol/LBaCl2溶液中Cl-的物质的量浓度为0.2mol/L,Ba2+的物质的量为0.002mol.
I.20mL0.1mol/LBaCl2溶液中Cl-的物质的量浓度为0.2mol/L,Ba2+的物质的量为0.002mol.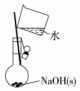
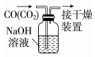

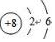 .A+、C2-、D-中离子半径最小的是Na+.(用具体离子符号表示)
.A+、C2-、D-中离子半径最小的是Na+.(用具体离子符号表示) _.
_.