题目内容
储存浓硫酸的铁罐外口出现严重的腐蚀现象,这体现了浓硫酸的( )
| A、脱水性和吸水性 |
| B、吸水性和酸性 |
| C、强氧化性和吸水性 |
| D、不挥发性和酸性 |
考点:浓硫酸的性质
专题:
分析:依据浓硫酸具有吸水性和酸性,稀硫酸与铁反应生成硫酸亚铁和氢气解答.
解答:
解:浓硫酸具有强的氧化性、吸水性、酸性,因为浓硫酸的强氧化性,常温下能够使铁铝发生钝化,阻止铁与浓硫酸继续反应,但是浓硫酸具有吸水性,吸收空气中水分浓度变稀,稀硫酸与铁反应生成硫酸亚铁和氢气,体现硫酸的酸性,
故选:B.
故选:B.
点评:本题考查了元素化合物知识,明确浓硫酸的性质是解题关键,注意对基础知识的积累.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
如表数据是对应物质的熔点,有关的判断错误的是( )
| Na2O | Na | AlF3 | AlCl3 | Al2O3 | BCl3 | CO2 | SiO2 |
| 920℃ | 97.8℃ | 1291℃ | 190℃ | 2073℃ | -107℃ | -57℃ | 1723℃ |
| A、金属晶体的熔点不一定比分子晶体的高 |
| B、AlCl3可能形成共价化合物分子 |
| C、含有金属阳离子的晶体就一定是离子晶体 |
| D、同族元素的氧化物可形成不同类型的晶体 |
已知X、Y、Z为三种原子序数相连的元素,最高价氧化物对应水化物的酸性相对强弱是:HXO4>H2YO4>H3ZO4.则下列说法正确的是( )
| A、气态氢化物的稳定性:HX>H2Y>ZH3 |
| B、非金属性:Y<X<Z |
| C、原子半径:X>Y>Z |
| D、原子序数:Z>Y>X |
大理石是一种重要的化工原料,其主要成分可以反应生成一系列物质,如下图所示.
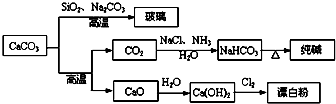
下列说法正确的是( )

下列说法正确的是( )
| A、Cl2和SO2均可以漂白有色物质,且漂白的原理相同 | ||||
B、由SiO2+Na2CO3
| ||||
| C、向饱和碳酸钠溶液中通入过量CO2,溶液变浑浊 | ||||
| D、制取玻璃和漂白粉所涉及的反应都是非氧化还原反应 |
漂白粉可由Cl2通入消石灰中制备.漂白粉的有效成分是( )
| A、Ca(OH)2 |
| B、CaCl2 |
| C、Ca(ClO)2 |
| D、CaCO3 |
下列常见的反应,在理论上不能用于设计原电池的是( )
| A、H2SO4(aq)+BaCI2(aq)═2HCl(aq)+BaSO4(s) |
| B、CH3CH2OH(l)+3O2(g)═2CO2(g)+3H2O(l) |
| C、4Fe(OH)2(S)+2H2O(l)+O2(g)═4Fe(OH)3 |
| D、2H2(g)+O2(g)═2H2O(l) |
下列各组粒子中质子数和电子数均相同的是( )
| A、CH4、H2O、Na+ |
| B、F2、Ar、HCl |
| C、H3O+、NH4+、Na |
| D、O2-、Mg2+、Ne |
 化学能和电能的相互转化,是能量转化的重要方式之一,如图两个实验装置是实现化学能和电能相互转化的装置.
化学能和电能的相互转化,是能量转化的重要方式之一,如图两个实验装置是实现化学能和电能相互转化的装置. :
: :
: