题目内容
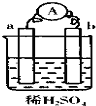 在如图所示的装置中,a的金属性比氢要强,b为碳棒,关于此装置的各种叙述不正确的是( )
在如图所示的装置中,a的金属性比氢要强,b为碳棒,关于此装置的各种叙述不正确的是( )分析:该原电池中,较活泼的金属a作负极,b碳棒作正极,负极上失电子发生氧化反应,正极上氢离子得电子发生还原反应,电子从负极沿导线流向正极.
解答:解:A.碳棒作正极,正极上氢离子得电子生成氢气,所以溶液酸性变弱,故A正确;
B.该原电池中,较活泼的金属a易失电子作负极,b碳棒作正极,故B正确;
C.该原电池中,较活泼的金属a作负极,b碳棒作正极,电子从负极a流向正极b,故C正确;
D.a是负极,负极上失电子发生氧化反应,故D错误;
故选D.
B.该原电池中,较活泼的金属a易失电子作负极,b碳棒作正极,故B正确;
C.该原电池中,较活泼的金属a作负极,b碳棒作正极,电子从负极a流向正极b,故C正确;
D.a是负极,负极上失电子发生氧化反应,故D错误;
故选D.
点评:本题考查了原电池工作原理.原电池中正负极的判断不能仅凭金属的活泼性判断,要根据电极反应的反应类型、电子的流向等方面判断.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案
相关题目
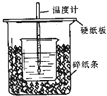 用50mL 0.50mol/L盐酸与50mL 0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL 0.50mol/L盐酸与50mL 0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: 用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: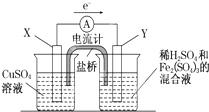 金属铜不溶于稀硫酸,可溶于铁盐溶液生成铜盐与亚铁盐.现将一定量的铜片加入到100mL稀硫酸和硫酸铁的混合溶液中,铜片完全溶解(不考虑盐的水解及溶液体积的变化).
金属铜不溶于稀硫酸,可溶于铁盐溶液生成铜盐与亚铁盐.现将一定量的铜片加入到100mL稀硫酸和硫酸铁的混合溶液中,铜片完全溶解(不考虑盐的水解及溶液体积的变化).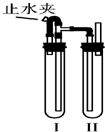 在如图所示的装置中,用NaOH溶液、铁屑、稀H2SO4制备Fe(OH)2白色沉淀.
在如图所示的装置中,用NaOH溶液、铁屑、稀H2SO4制备Fe(OH)2白色沉淀.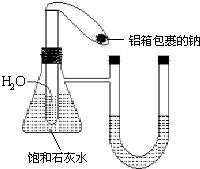 在如图所示的装置中,锥形瓶中装有饱和石灰水,小试管中装有一定量的水,气球中有一小块用铝箔包着的钠,整套装置气密性良好,未反应前U形管两端液面相平.现将气球中的金属钠放入小试管中与水反应.
在如图所示的装置中,锥形瓶中装有饱和石灰水,小试管中装有一定量的水,气球中有一小块用铝箔包着的钠,整套装置气密性良好,未反应前U形管两端液面相平.现将气球中的金属钠放入小试管中与水反应.