题目内容
某溶液中含有两种溶质AlCl3和H2SO4,它们的物质的量之比为2:1.用石墨做电极电解该混合溶液时,根据电极产物,可分为若干个阶段,下列叙述不正确的是( )
| A、阴极自始至终只有H2 |
| B、阳极先析出Cl2后析出O2 |
| C、电解最后阶段为电解水 |
| D、溶液中先有白色沉淀生成后沉淀全部溶解 |
考点:电解原理
专题:电化学专题
分析:电解氯化铝和硫酸的混合液,阳极上氯离子放电,然后是氢氧根离子放电;阴极上始终是氢离子放电,即电解时先电解氯化氢,最后阶段为电解水,根据原理来回答.
解答:
解:A.阴极上氢离子放电,所以阴极自始至终只有H2析出,故A正确;
B.阳极上氯离子先放电然后氢氧根离子放电,所以阳极先析出Cl2后析出O2,故B正确;
C.电解时先电解氯化氢,最后阶段为电解水,故C正确;
D.电解时先电解氯化氢,最后阶段为电解水,所以溶液中始终没有白色沉淀,故D错误;
故选D.
B.阳极上氯离子先放电然后氢氧根离子放电,所以阳极先析出Cl2后析出O2,故B正确;
C.电解时先电解氯化氢,最后阶段为电解水,故C正确;
D.电解时先电解氯化氢,最后阶段为电解水,所以溶液中始终没有白色沉淀,故D错误;
故选D.
点评:本题考查学生电解池的工作原理知识,注意离子的放电顺序是解题的关键,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
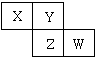 如图是元素周期表的一部分.X、Y、Z、W均为短周期元素,若W原子最外电子层电子数是其内层电子数的
如图是元素周期表的一部分.X、Y、Z、W均为短周期元素,若W原子最外电子层电子数是其内层电子数的| 7 |
| 10 |
| A、X元素的氢化物水溶液呈碱性 |
| B、气态氢化物的稳定性:Y>Z |
| C、最高氧化物对应水化物的酸性:W>Z |
| D、阴离子半径从大到小排列的顺序:Y>Z>W |
不属于氧化还原反应的是( )
A、2Al+Fe2O3
| ||||
B、2Mg+CO2
| ||||
C、N2+3H2
| ||||
| D、CaO+H2O═Ca(OH)2 |
下列实验操作不正确的是( )
| A、NaCl溶液蒸发结晶时,蒸发皿中有晶体析出并剩余少量液体时即停止加热 |
| B、除去Fe(OH)3胶体中混有的Cl-离子,可用渗析的方法 |
| C、蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
| D、用四氯化碳萃取碘时,碘的四氯化碳溶液从分液漏斗上口倒出 |
下列说法正确的是( )
| A、根据交叉分类法,Na2SO4既是钠盐又是硫酸盐 |
| B、氧化还原反应中有一种元素化合价升高,必定有另一种元素化合价降低 |
| C、根据是否有丁达尔效应将分散系分为溶液、胶体和浊液 |
| D、稀H2SO4能导电,所以稀H2SO4是电解质 |
铝是重要的金属材料之一,下列关于铝的叙述中,不正确的是( )
| A、铝原子最外层有3个电子 |
| B、铝是地壳中含量最多的金属元素 |
| C、在常温下,铝不能与氧气反应 |
| D、铝易被氧化,而Al3+则很难被还原 |
下列物质中,既有离子键又有非极性键的化合物是( )
| A、NH4Cl |
| B、Na2O2 |
| C、CO2 |
| D、MgCl2 |
不能作为比较元素原子得失电子能力相对强弱的依据是( )
| A、元素气态氢化物的稳定性 |
| B、元素单质熔、沸点高低 |
| C、金属间发生的置换 |
| D、非金属阴离子的还原性强弱 |