题目内容
3.NaNO2是一种食品添加剂,它能致癌.酸性高锰酸钾溶液与亚硝酸钠的反应方程式是:MnO4-+NO2-+H+→Mn2++NO3-+H2O.下列叙述中正确的是( )| A. | NaNO2既具有氧化性又具有还原性 | |
| B. | 该反应中NO2-被还原 | |
| C. | 反应过程中溶液的pH变小 | |
| D. | 生成1molNaNO3需要消耗0.6molKMnO4 |
分析 MnO4-+NO2-+H+→Mn2++NO3-+H2O中,Mn元素的化合价降低,N元素的化合价升高,以此来解答.
解答 解:A.NaNO2中N元素的化合价为+3价,为中间价,既具有氧化性又具有还原性,故A正确;
B.该反应中N元素的化合价升高,则NO2-被氧化,故B错误;
C.反应消耗氢离子,pH增大,故C错误;
D.由电子及原子守恒可知,生成1molNaNO3需要消耗$\frac{1mol×(5-3)}{(7-2)}$=0.4molKMnO4,故D错误;
故选A.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意电子守恒的应用及常见元素化合价判断,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.如图选用的相关仪器(固定装置略去)符合实验要求的是( )
| A. |  存放浓硝酸 | B. | 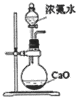 可用于制备氨气 | ||
| C. | 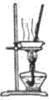 蒸干氯化铝溶液AlCl3•6H2O晶体 | D. |  实验室抽取乙烯 |
14.下列过程中,发生氧化还原反应的是( )
| A. | Cu和稀HNO3反应 | B. | Fe导电 | ||
| C. | Na2CO3溶液与盐酸反应 | D. | 实验室制取NH3 |
11.用固体氢氧化钠配制一定物质的量浓度溶液时,下列说法正确的是( )
| A. | 称量固体氢氧化钠时托盘天平两边放大小一样的白纸 | |
| B. | 配置溶液时洗涤烧杯和玻璃棒,引起所得溶液浓度偏高 | |
| C. | 容量瓶使用前未经干燥会导致所得溶液浓度偏低 | |
| D. | 容量瓶、分液漏斗、滴定管使用前都要检查是否漏水 |
18.下列化学药品中属有毒且易燃料是( )
| A. | 乙酸 | B. | 氰化钾 | C. | 甲醇 | D. | 氢气 |
8.某混合气体可能含有Cl2、O2、SO2、NO、NO2中的两种或多种气体.现将此无色的混合气体通过品红溶液后,品红溶液褪色,把剩余气体排入空气中,很快变为红棕色.对于原混合气体成分的判断中正确的是( )
| A. | 肯定有SO2和NO | B. | 肯定只有NO | ||
| C. | 可能有Cl2和O2 | D. | 肯定没有Cl2、NO2,可能有O2 |
15.对溶液中的离子反应存在下列几种说法,其中正确的是( )
| A. | 不可能是氧化还原反应 | B. | 只能是复分解反应 | ||
| C. | 可能是置换反应 | D. | 不可能是化合反应 |
12.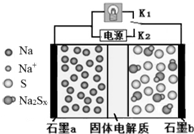 高温钠硫电池是一种新型可充电电池,其工作原理如图所示,图中固体电解质是Na+导体.下列叙述正确的是( )
高温钠硫电池是一种新型可充电电池,其工作原理如图所示,图中固体电解质是Na+导体.下列叙述正确的是( )
 高温钠硫电池是一种新型可充电电池,其工作原理如图所示,图中固体电解质是Na+导体.下列叙述正确的是( )
高温钠硫电池是一种新型可充电电池,其工作原理如图所示,图中固体电解质是Na+导体.下列叙述正确的是( )| A. | 放电时,石墨电极a为正极 | |
| B. | 放电时,Na+从石墨b向石墨a方向迁移 | |
| C. | 可将装置中的固体电解质改成NaCl溶液 | |
| D. | 充电时,b极反应为Na2Sx-2e-=xS+2Na+ |
13.某学生用NaHCO3和KHCO3组成的某混合物进行实验,测得如下数据(盐酸的物质的量浓度相等),下列有关的说法中,不正确的是( )
| 实验序号 | 1 | 2 | 3 |
| V(盐酸)/mL | 50 | 50 | 50 |
| m(混合物)/g | 9.2 | 15.7 | 27.6 |
| V(CO2)(标准状况)/L | 2.24 | 3.36 | 3.36 |
| A. | 实验②中,混合物过量 | |
| B. | 原混合物样品中n(NaHCO3):n(KHCO3)=1:1 | |
| C. | 盐酸的物质的量浓度为2mol•L-1 | |
| D. | 实验反应后,至少需继续加入50mL的盐酸溶液才能使27.6g的混合物全部反应 |