题目内容
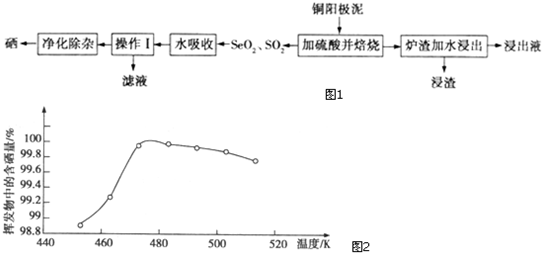
11.利用铝灰(主要成分为Al、Al2O3、AlN、FeO等)制备铝鞣剂[主要成分为Al(OH2Cl)]的一种工艺如下:
(1)气体A能使湿润的红色石蕊试纸变蓝.铝灰在90℃水解生成A的化学方程式为+3H2O$\frac{\underline{\;90℃\;}}{\;}$Al(OH)3+NH3↑;“水解”采用90℃而不在室温下进行的原因是降低NH3在水中的溶解度,促使NH3逸出.
(2)“酸溶”时,Al2O3发生反应的离子方程为Al2O3+6H+═2Al3++3H2O.
(3)“氧化”时,发生反应的离子方程式为2Fe2++2H++ClO-═2Fe3++Cl-+H2O.
(4)“废渣”成分为Fe(OH)3(填化学式).
(5)采用喷雾干燥而不用蒸发的原因是防止Al(OH)2Cl水解生成Al(OH)3.
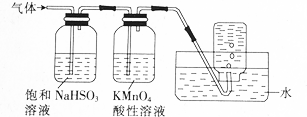
(6)煅烧硫酸铝铵晶体,发生的主要反应是:4[NH4Al(SO4)2•12H2O]$\frac{\underline{\;1240℃\;}}{\;}$2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O,将产生的气体通过如图所示的装置.则
①集气瓶中收集到的气体是N2(填化学式).
②足量饱和NaHSO3溶液吸收的物质除大部分H2O(g)外还有NH3、SO3(填化学式)
分析 铝灰主要成分为Al、Al2O3、AlN、FeO等加入水发生反应,AlN和水反应生成氢氧化铝和氨气,加入盐酸酸溶后,生成氯化铝溶液和氯化亚铁溶液,加入漂白剂氧化亚铁离子为铁离子,加入纯碱调节溶液PH使铁笼子全部沉淀,采用喷雾干燥制备铝鞣剂;
(1)气体A能使湿润的红色石蕊试纸变蓝,说明生成的是氨气,铝灰中的AlN和水发生水解反应生成氢氧化铝沉淀和氨气,加热可以促进氮化铝水解生成氨气;
(2)氧化铝是两性氧化物酸溶时和盐酸发生反应生成氯化铝溶液;
(3)加入漂白液的作用是利用次氯酸根离子在酸溶液中的强氧化性氧化亚铁离子为铁离子;
(4)上述分析可知滤渣为氢氧化铁沉淀;
(5)铝鞣剂主要成分为Al(OH)2Cl;
(6)生成气体中,饱和亚硫酸氢钠可吸收氨气、三氧化硫,高锰酸钾吸收二氧化硫,最后吸收氮气.
解答 解:铝灰主要成分为Al、Al2O3、AlN、FeO等加入水发生反应,AlN和水反应生成氢氧化铝和氨气,加入盐酸酸溶后,生成氯化铝溶液和氯化亚铁溶液,加入漂白剂氧化亚铁离子为铁离子,加入纯碱调节溶液PH使铁笼子全部沉淀,采用喷雾干燥制备铝鞣剂;
(1)气体A能使湿润的红色石蕊试纸变蓝,说明生成的是氨气,铝灰中的AlN和水发生水解反应生成氢氧化铝沉淀和氨气,反应的化学方程式为:AlN+3H2O$\frac{\underline{\;90℃\;}}{\;}$Al(OH)3+NH3↑,加热可以促进氮化铝水解生成氨气,降低NH3在水中的溶解度,促使NH3逸出;
故答案为:+3H2O$\frac{\underline{\;90℃\;}}{\;}$Al(OH)3+NH3↑;降低NH3在水中的溶解度,促使NH3逸出;
(2)氧化铝是两性氧化物酸溶时和盐酸发生反应生成氯化铝溶液,)“酸溶”时,Al2O3发生反应的离子方程式为:Al2O3+6H+═2Al3++3H2O;
故答案为:Al2O3+6H+═2Al3++3H2O;
(3)加入漂白液的作用是利用次氯酸根离子在酸溶液中的强氧化性氧化亚铁离子为铁离子,反应的离子方程式为:2Fe2++2H++ClO-═2Fe3++Cl-+H2O;
故答案为:2Fe2++2H++ClO-═2Fe3++Cl-+H2O;
(4)上述分析可知“废渣”成分为氢氧化铁沉淀,化学式为:Fe(OH)3,
故答案为:Fe(OH)3;
(5)铝鞣剂主要成分为Al(OH)2Cl,在加热蒸发时会发生水解,为防止水解利用喷雾干燥,减少铝鞣剂水解,
故答案为:防止Al(OH)2Cl水解生成Al(OH)3;
(6)①生成气体中,饱和亚硫酸氢钠可吸收氨气、三氧化硫,高锰酸钾吸收二氧化硫,最后吸收氮气,
故答案为:N2;
②NH3、SO3能够与亚硫酸氢钠反应,所以足量饱和NaHSO3溶液吸收的物质除大部分H2O(g)外还有NH3、SO3,
故答案为:NH3、SO3.
点评 本题考查了物质制备的实验流程分析判断、物质性质的理解应用,为高频考点,题目难度中等,侧重于学生的分析、实验能力的考查,注意把握工艺流程和反应产物的分析,掌握常见元素化合物知识,试题培养了学生的分析能力及化学实验能力.

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案| 元素 | A | B | C | D |
| 性质 或结 构信息 | 原子核外有两个电子层,最外层有3个未成对电子 | 原子的M层有1对成对的p电子 | 原子核外电子排布为:[Ar]3 d104sx,有+1、+2两种常见化合价 | 有两种常见氧化物,其中一种是冶炼金属工业的常用还原剂 |
(2)B元素的低价氧化物分子中心原子的杂化方式为sp2杂化,B元素的最高价氧化物分子的VSEPR构型为平面三角形;B元素与D元素形成分子空间构型为直线形;
(3)D元素最高价氧化物的熔点比同主族相邻元素最高价氧化物的熔点低(填“高”或“低”),其原因是CO2是分子晶体,SiO2是原子晶体;
(4)往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,观察到的现象为先生成蓝色沉淀,后沉淀溶解,最后得到深蓝色溶液;后一现象的离子方程式为:Cu(OH)2+4NH3•H2O═[Cu(NH3)4]2++4H2O+2OH-.
(5)C晶体的堆积方式如图所示
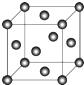 ,设晶胞边长为a cm,阿伏伽德罗常数用NA表示,则晶胞中C原子的配位数为12,C晶体的密度为$\frac{4×64}{{a}^{3}×{N}_{A}}$g•cm-3(要求写表达式,可以不简化).
,设晶胞边长为a cm,阿伏伽德罗常数用NA表示,则晶胞中C原子的配位数为12,C晶体的密度为$\frac{4×64}{{a}^{3}×{N}_{A}}$g•cm-3(要求写表达式,可以不简化). | A. | 元素非金属性由强到弱的顺序是:Z>Y>X | |
| B. | Y元素最高价氧化物对应水化物的化学式可表示为H4YO4 | |
| C. | 3种元素的气态氢化物中,Z的气态氢化物最稳定 | |
| D. | 原子半径由大到小的顺序为 Z>Y>X |
| A. | 1.0 L 1.0 mol•L-1的NaAlO2水溶液中含有的氧原子数为2NA | |
| B. | 23 g Na与足量H2O反应完全后可生成NA个H2分子 | |
| C. | 标准状况下,11.2 L CH3CH2OH中含有的分子数目为0.5NA | |
| D. | 常温常压下,46 g的NO2与N2O4混合物含有的原子数为3 NA |
(1)常温下0.1mol/L的CH3COOH溶液加水稀释过程,下列表达式的数据一定变小的是A.
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ C.c(H+)•c(OH-) D.$\frac{c(O{H}^{-})}{c({H}^{+})}$
(2)取10mL的乙溶液,加入等体积的水,醋酸的电离平衡向右(填“向左”、“向右”或“不”)移动;另取10mL的乙溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中c(H+)/c(CH3COOH)的比值将减小(填“增大”、“减小”或“无法确定”).
(3)相同条件下,取等体积的甲、乙两溶液,各稀释100倍.稀释后的溶液,其pH大小关系为:pH(甲)>pH(乙)( 填“>”、“<”或“=”).
(4)取等体积的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和,则消耗的NaOH溶液的体积大小关系为:V(甲)< V(乙)( 填“>”、“<”或“=”).
(5)已知25℃时,两种酸的电离平衡常数如下:
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数K1 | 1.8×10-5 | 4.3×10-7 | 3.0×10-8 |
| K2 | -- | 5.6×10-11 | -- |
A.HCO3- B.CO32- C.ClO- D.CH3COO-
写出下列反应的离子方程式:CH3COOH+Na2CO3(少量):2CH3COOH+CO32-=H2O+2CH3COO-+CO2↑;HClO+Na2CO3(少量):HClO+CO32-=ClO-+HCO3-.
| A. | H+、Fe2+、I-、NO3- | B. | Al3+、AlO2-、SO42-、Cl- | ||
| C. | K+、Ag+、Ca2+、NO3- | D. | NH4+、Na+、OH-、MnO4- |
| A. | 1mol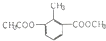 能与4molNaOH充分反应 能与4molNaOH充分反应 | |
| B. |  系统命名法为3-丁烯 系统命名法为3-丁烯 | |
| C. |  的碳原子都在一个平面内,且它的二氯代物为3种 的碳原子都在一个平面内,且它的二氯代物为3种 | |
| D. | 1mol 可以与4molH2发生加成 可以与4molH2发生加成 |