题目内容
X、Y、Z是短周期元素的单质,A、B是它们的化合物.物质之间的转化关系如图(其中反应条件和某些生成物已略去):
(1)如果X、Y组成元素是同主族元素时,按下列要求分别写出“A+X=B+Y”的反应方程式:
①若B为水,则反应方程式为 .
②已知A、B都是氧化物,则反应方程式为 .
(2)如果X、Y组成元素不是同主族元素时,按下列要求分别写出X、Y的化学式和对应的化学方程式.
①若X的组成元素是地壳中含量最多的金属元素,则X为 Z为 .写出对应的化学方程式 .
②若Y的组成元素在自然界中形成化合物种类最多,则X为 Z为 .写出对应的化学方程式 .

(1)如果X、Y组成元素是同主族元素时,按下列要求分别写出“A+X=B+Y”的反应方程式:
①若B为水,则反应方程式为
②已知A、B都是氧化物,则反应方程式为
(2)如果X、Y组成元素不是同主族元素时,按下列要求分别写出X、Y的化学式和对应的化学方程式.
①若X的组成元素是地壳中含量最多的金属元素,则X为
②若Y的组成元素在自然界中形成化合物种类最多,则X为

考点:无机物的推断
专题:推断题,元素周期律与元素周期表专题
分析:X、Y、Z是短周期元素的单质,A、B是它们的化合物,
(1)如果X、Y组成元素是同主族元素时,符合“A+X=B+Y”的反应方程式,
①A+X=B+Y为置换反应,若B为水,X、Z为氢气、氧气,如果X是氢气,氢气和化合物发生置换反应不能生成Na,所以X不是氢气,应该是氧气,则Y是S,Z为氢气,所以A是H2S;
②A+X=B+Y为置换反应,X、Y、Z为单质,X和A发生置换反应生成Y,则X具有还原性,如果X为氢气,X能和Z反应生成氧化物B,则Z是氧气,Y是单质,能生成氧化物A,且X、Y属于同一主族元素,具有还原性且符合条件的X为C、Y为Si,A为SiO2、B为CO;
(2)X、Y组成元素不是同主族元素时,
①若X的组成元素是地壳中含量最多的金属元素,则X是Al,A+X=B+Y为置换反应,X具有还原性,能和酸、强碱溶液发生置换反应,则Y为氢气,A为酸或碱,如果A是酸,这几种元素都是短周期元素,所以A应该是HCl,B为AlCl3;
②若Y的组成元素在自然界中形成化合物种类最多,则Y是C,A+X=B+Y为置换反应,X具有还原性,能和氧化物反应生成C单质的短周期元素单质为Mg,所以X是Mg、Z为氧气、A是CO2、B是MgO.
(1)如果X、Y组成元素是同主族元素时,符合“A+X=B+Y”的反应方程式,
①A+X=B+Y为置换反应,若B为水,X、Z为氢气、氧气,如果X是氢气,氢气和化合物发生置换反应不能生成Na,所以X不是氢气,应该是氧气,则Y是S,Z为氢气,所以A是H2S;
②A+X=B+Y为置换反应,X、Y、Z为单质,X和A发生置换反应生成Y,则X具有还原性,如果X为氢气,X能和Z反应生成氧化物B,则Z是氧气,Y是单质,能生成氧化物A,且X、Y属于同一主族元素,具有还原性且符合条件的X为C、Y为Si,A为SiO2、B为CO;
(2)X、Y组成元素不是同主族元素时,
①若X的组成元素是地壳中含量最多的金属元素,则X是Al,A+X=B+Y为置换反应,X具有还原性,能和酸、强碱溶液发生置换反应,则Y为氢气,A为酸或碱,如果A是酸,这几种元素都是短周期元素,所以A应该是HCl,B为AlCl3;
②若Y的组成元素在自然界中形成化合物种类最多,则Y是C,A+X=B+Y为置换反应,X具有还原性,能和氧化物反应生成C单质的短周期元素单质为Mg,所以X是Mg、Z为氧气、A是CO2、B是MgO.
解答:
解:X、Y、Z是短周期元素的单质,A、B是它们的化合物,
(1)如果X、Y组成元素是同主族元素时,符合“A+X=B+Y”的反应方程式,
①A+X=B+Y为置换反应,若B为水,X、Z为氢气、氧气,如果X是氢气,氢气和化合物发生置换反应不能生成Na,所以X不是氢气,应该是氧气,则Y是S,Z为氢气,所以A是H2S,则该反应方程式为2H2S+O2=2S+2H2O,
故答案为:2H2S+O2=2S+2H2O;
②A+X=B+Y为置换反应,X、Y、Z为单质,X和A发生置换反应生成Y,则X具有还原性,如果X为氢气,X能和Z反应生成氧化物B,则Z是氧气,Y是单质,能生成氧化物A,且X、Y属于同一主族元素,具有还原性且符合条件的X为C、Y为Si,A为SiO2、B为CO,则该反应方程式为SiO2+2C
Si+2CO,
故答案为:SiO2+2C
Si+2CO;
(2)X、Y组成元素不是同主族元素时,
①若X的组成元素是地壳中含量最多的金属元素,则X是Al,A+X=B+Y为置换反应,X具有还原性,能和酸、强碱溶液发生置换反应,则Y为氢气,A为酸或碱,如果A是酸,这几种元素都是短周期元素,所以A应该是HCl,B为AlCl3,该反应方程式为2Al+6HCl=2AlCl3+3H2↑,
故答案为:Al;Cl2;2Al+6HCl=2AlCl3+3H2↑;
②若Y的组成元素在自然界中形成化合物种类最多,则Y是C,A+X=B+Y为置换反应,X具有还原性,能和氧化物反应生成C单质的短周期元素单质为Mg,所以X是Mg、Z为氧气、A是CO2、B是MgO,该反应为2Mg+CO2
2MgO+C,
故答案为:Mg;O2;2Mg+CO2
2MgO+C.
(1)如果X、Y组成元素是同主族元素时,符合“A+X=B+Y”的反应方程式,
①A+X=B+Y为置换反应,若B为水,X、Z为氢气、氧气,如果X是氢气,氢气和化合物发生置换反应不能生成Na,所以X不是氢气,应该是氧气,则Y是S,Z为氢气,所以A是H2S,则该反应方程式为2H2S+O2=2S+2H2O,
故答案为:2H2S+O2=2S+2H2O;
②A+X=B+Y为置换反应,X、Y、Z为单质,X和A发生置换反应生成Y,则X具有还原性,如果X为氢气,X能和Z反应生成氧化物B,则Z是氧气,Y是单质,能生成氧化物A,且X、Y属于同一主族元素,具有还原性且符合条件的X为C、Y为Si,A为SiO2、B为CO,则该反应方程式为SiO2+2C
| ||
故答案为:SiO2+2C
| ||
(2)X、Y组成元素不是同主族元素时,
①若X的组成元素是地壳中含量最多的金属元素,则X是Al,A+X=B+Y为置换反应,X具有还原性,能和酸、强碱溶液发生置换反应,则Y为氢气,A为酸或碱,如果A是酸,这几种元素都是短周期元素,所以A应该是HCl,B为AlCl3,该反应方程式为2Al+6HCl=2AlCl3+3H2↑,
故答案为:Al;Cl2;2Al+6HCl=2AlCl3+3H2↑;
②若Y的组成元素在自然界中形成化合物种类最多,则Y是C,A+X=B+Y为置换反应,X具有还原性,能和氧化物反应生成C单质的短周期元素单质为Mg,所以X是Mg、Z为氧气、A是CO2、B是MgO,该反应为2Mg+CO2
| ||
故答案为:Mg;O2;2Mg+CO2
| ||
点评:本题考查无机物推断,侧重考查学生分析、推断能力,同时考查学生发散思维能力,常见的置换反应有:金属置换金属、金属置换非金属、非金属置换非金属、非金属置换金属,题目难度中等.

练习册系列答案
相关题目
X、Y、Z、W为四种短周期主族元素.其中X、Z同族,Y、Z同周期,W与X、Y既不同族也不同周期;X原子最外层电子数是核外电子层数的3倍;Y的最高正价与最低负价的代数和为6.下列说法正确的是( )
| A、Y元素最高价氧化物对应水化物的化学式为HYO4 |
| B、原子半径由小到大的顺序为:W>X>Z |
| C、Z元素可以形成两种酸性氧化物 |
| D、Y、Z两元素的气态氢化物中,Z的气态氢化物最稳定 |
下列电离方程式错误的是( )
| A、Na2CO3=2Na++CO32- |
| B、NaHSO4=Na++H++SO42- |
| C、NaHCO3=Na++HCO3- |
| D、KClO3=K++Cl-+3O2- |
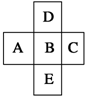 在元素周期表中的前四周期,两两相邻的5种元素如图所示,若B元素的核电荷数为a.下列说法正确的是( )
在元素周期表中的前四周期,两两相邻的5种元素如图所示,若B元素的核电荷数为a.下列说法正确的是( )| A、B、D的原子序数之差可能为2 |
| B、E、B的原子序数之差可能是8、18或32 |
| C、5种元素的核电荷总数之和可能为5a+10 |
| D、A、E的原子序数之差可能是7 |
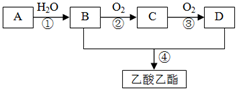 已知:A是石油裂解气的主要成分,A的产量通常用来衡量一个国家的石油化工水平.现以A为主要原料合成乙酸乙酯,其合成路线如图所示.回答下列问题:
已知:A是石油裂解气的主要成分,A的产量通常用来衡量一个国家的石油化工水平.现以A为主要原料合成乙酸乙酯,其合成路线如图所示.回答下列问题: 为测定放置一段时间的小苏打样品中纯碱的质量分数,某化学兴趣小组设计如下实验方案:
为测定放置一段时间的小苏打样品中纯碱的质量分数,某化学兴趣小组设计如下实验方案: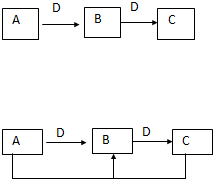 在一定条件下进行下列化学反应,请根据以下的转化关系回答下列问题(注:A、B、C中均含有同一种元素):
在一定条件下进行下列化学反应,请根据以下的转化关系回答下列问题(注:A、B、C中均含有同一种元素):