题目内容
下列物质的立体结构与NH3相同的是( )
| A、H2O |
| B、CH4 |
| C、CO2 |
| D、H3O+ |
考点:判断简单分子或离子的构型
专题:化学键与晶体结构
分析:氨气分子中N原子价层电子对个数=3+
×(5-3×1)=4且含有一个孤电子对,则氨气分子是三角锥形结构,物质的立体结构和氨气分子相同,说明该分子也是三角锥形结构,根据价层电子对互斥理论来分析解答.
| 1 |
| 2 |
解答:
氨气分子中N原子价层电子对个数=3+
×(5-3×1)=4且含有一个孤电子对,则氨气分子是三角锥形结构,物质的立体结构和氨气分子相同,说明该分子也是三角锥形结构,
A.水分子中O原子价层电子对个数=2+
×(6-2×1)=4且含有2个孤电子对,所以水分子为V形,故A错误;
B.甲烷分子中C原子价层电子对个数=4+
×(4-4×1)=4且不含孤电子对,所以甲烷分子为正四面体结构,故B错误;
C.二氧化碳分子中C原子和每个O原子形成共价双键,且不含孤电子对,所以二氧化碳分子为直线形分子,故C错误;
D.水合氢离子中O原子价层电子对个数=3+
×(6-1-3×1)=4且含有一个孤电子对,所以为三角锥形结构,故D正确;
故选D.
| 1 |
| 2 |
A.水分子中O原子价层电子对个数=2+
| 1 |
| 2 |
B.甲烷分子中C原子价层电子对个数=4+
| 1 |
| 2 |
C.二氧化碳分子中C原子和每个O原子形成共价双键,且不含孤电子对,所以二氧化碳分子为直线形分子,故C错误;
D.水合氢离子中O原子价层电子对个数=3+
| 1 |
| 2 |
故选D.
点评:本题考查了分子空间构型的判断,根据价层电子对互斥理论来分析解答即可,注意孤电子对的计算方法,题目难度不大.

练习册系列答案
相关题目
在给定条件下,下列划横线的物质在化学反应中能被完全消耗的是( )
| A、标准状况下,将1g铝片投入20mL 18.4mol?L-1的硫酸中 |
| B、向100mL3moI?L-1的硝酸中加入5.6g铁 |
| C、用50mL18mol?L-1浓硫酸与足量Cu共热(指其中的硫酸被完全消耗) |
| D、在5×107 Pa、500℃和铁触媒催化的条件下,用3mol氢气和2mol氮气合成氨 |
根据热化学方程式S(s)+O2(g)═SO2(g)△H=-297.23kJ?mol-1,分析下列说法正确的是( )
| A、S(g)+O2(g)═SO2(g)|△H|=297.23 kJ?mol-1 |
| B、S(g)+O2(g)═SO2(g)|△H|<297.23 kJ?mol-1 |
| C、1 mol SO2(g)所具有的能量大于1 mol S(s)与1 mol O2(g)所具有的能量之和 |
| D、1 mol SO2(g)所具有的能量小于1 mol S(s)与1 mol O2(g)所具有的能量之和 |
有机化合物Y是合成有关药物的重要中间体,可由有机化合物X经多步反应制得.有关如图两种化合物的说法正确的是( )
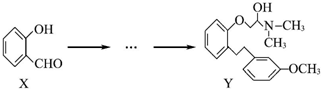

| A、1molX最多能与4molH2发生加成反应 |
| B、在Y分子中只含有1个手性碳原子 |
| C、X、Y均可以与NaOH溶液发生反应 |
| D、Y能发生加成、取代、消去、水解反应 |
奥运会上发令枪所用“火药”的主要成分是氯酸钾和红磷,撞击时发生化学反应:5KClO3+6P=3P2O5十5KCl.而我国古代“火药”的成分是木炭粉(C)、硫磺(S)、硝石(KNO3),经点燃发生的反应为:S+2KNO3+3C=K2S+N2↑+3CO2↑,则下列有关叙述中错误的是( )
| A、两个反应中还原产物前者为KCl,后者为K2S和N2 |
| B、两个反应均为置换反应 |
| C、若两个反应中生成等物质的量的P2O5和CO2转移电子数之比为5:2 |
| D、火药中的钾盐均作氧化剂 |
在容积恒定的密闭容器中放入1mol A,2mol B,A(g)+2B?2Q(g)当达到平衡时测得压强减小
,则A的转化率为( )
| 1 |
| 6 |
| A、60% | B、50% |
| C、40% | D、30% |