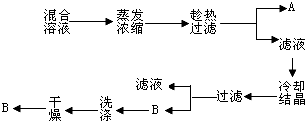
题目内容
除去下列物质中的少量的杂质,所用试剂和方法不正确的是( )
| 物质 | 杂质 | 除杂所用试剂和方法 | |
| A | CO2 | CO | 在氧气中点燃 |
| B | NaCl固体 | 泥沙 | 加水溶解、过滤、蒸发结晶 |
| C | Cu | Fe | 加稀盐酸溶解、过滤 |
| D | KCl | I2 | 加热 |
| A、A | B、B | C、C | D、D |
考点:物质的分离、提纯的基本方法选择与应用,物质的分离、提纯和除杂
专题:化学实验基本操作
分析:A.CO在二氧化碳中难燃烧,且易引入新杂质;
B.泥沙不溶于水,NaCl溶于水;
C.Fe与盐酸反应,而Cu不能;
D.碘易升华,而KCl不能.
B.泥沙不溶于水,NaCl溶于水;
C.Fe与盐酸反应,而Cu不能;
D.碘易升华,而KCl不能.
解答:
解:A.CO在二氧化碳中难燃烧,且易引入新杂质,不能除杂,应利用灼热的CuO来除杂,故A错误;
B.泥沙不溶于水,NaCl溶于水,则加水溶解、过滤、蒸发结晶可得到纯净的NaCl,故B正确;
C.Fe与盐酸反应,而Cu不能,则加稀盐酸溶解、过滤可得到Cu,故C正确;
D.碘易升华,而KCl不能,则加热可除杂,故D正确;
故选A.
B.泥沙不溶于水,NaCl溶于水,则加水溶解、过滤、蒸发结晶可得到纯净的NaCl,故B正确;
C.Fe与盐酸反应,而Cu不能,则加稀盐酸溶解、过滤可得到Cu,故C正确;
D.碘易升华,而KCl不能,则加热可除杂,故D正确;
故选A.
点评:本题考查混合物分离提纯方法的选择和应用,为高频考点,把握物质的性质及性质差异为解答的关键,侧重分离及除杂的考查,注意除杂的原则,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
实验是化学研究的基础,关于下列各实验装置图的叙述中,正确的是( )
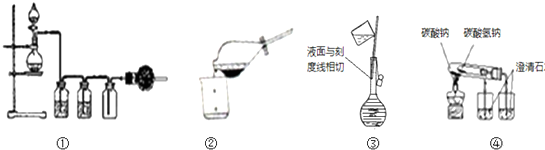

| A、①可用于实验室用MnO2固体与浓盐酸反应,制取并收集干燥、纯净的Cl2 |
| B、②从溴水中萃取溴后的分离操作 |
| C、③配制1mol/LNaCl溶液定容操作 |
| D、用图④操作可比较Na2CO3与NaHCO3的热稳定性 |
当光束通过下列分散系时,能产生丁达尔效应的是( )
| A、硫酸铜溶液 |
| B、氯化铁溶液 |
| C、氢氧化铁胶体 |
| D、氯化钠溶液 |
T℃时在2L容积不变的密闭容器中使X(g)与Y(g)发生反应生成Z(g).反应过程中X、Y、Z的浓度变化如图1所示.则下列结论正确的是( )
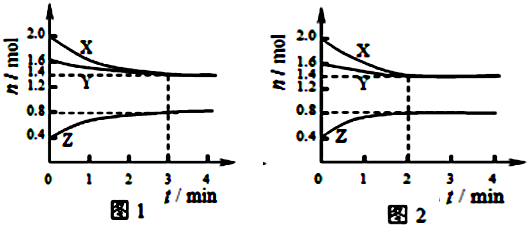

| A、容器中发生的反应可表示为:3X(g)+Y(g)?2Z(g) |
| B、反应进行前3min内,用X表示的反应速率v(X)=0.1mol/(L?min) |
| C、若改变反应条件,使反应进程如图2所示,则改变的条件是增大压强 |
| D、如图1所示,该反应达到化学平衡时,X的转化率为70% |
通以相等的电量,分别电解等浓度的硝酸银和硝酸亚汞(亚汞的化合价为+1)溶液,若被还原的硝酸银和硝酸亚汞的物质的量之比n(硝酸银):n(硝酸亚汞)=2:1,则下列叙述正确的是( )
| A、电解后溶液的pH都增大 |
| B、在两个阳极上得到的产物的物质的量不相等 |
| C、硝酸亚汞的分子式为Hg2(NO3)2 |
| D、在两个阴极上得到的银和汞的物质的量之比为2:1 |
下列各物质中,按熔点由高到低的顺序排列正确的是( )
| A、CH4>SiH4>GeH4>SnH4 |
| B、KCl>NaCl>NaF>LiF |
| C、Rb>K>Na>Li |
| D、金刚石>氯化钠>钠>干冰 |
下列有关物质用途的说法错误的是( )
| A、过氧化钠可用作潜水艇供氧剂 |
| B、氧化铝是一种耐火材料,可制耐高温实验材料 |
| C、氧化铁可用作红色油漆和涂料 |
| D、氢氧化铝、苏打等可用于治疗胃酸过多 |
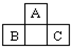 如图为短周期一部分.A、C两元素原子核外分别有两个、一个未成对电子.试回答:
如图为短周期一部分.A、C两元素原子核外分别有两个、一个未成对电子.试回答: