题目内容
已知-NH2连在苯环上显碱性,-CONH2连在苯环上显中性.现有分子式为C7H7O2N的有机物分子结构中有一个苯环和互为对位的两个侧链,试写出该分子式对应的符合下列条件的四种同分异构体的结构简式:
甲:既有酸性,又有碱性
乙:只有酸性
丙:既无酸性,又无碱性
丁:只有碱性 .
甲:既有酸性,又有碱性
乙:只有酸性
丙:既无酸性,又无碱性
丁:只有碱性
考点:有机物的推断
专题:有机物的化学性质及推断
分析:分子式为C7H7O2N的有机物分子结构中有一个苯环和互为对位的两个侧链,甲既有酸性又有碱性,则A含有侧链为-NH2、-COOH;乙只有酸性,则乙含有侧链为-OH、-CONH2;丙既无酸性又无碱性,则丙中侧链为-CH3、-NO2;丁只有碱性,则丁中侧链为-NH2、-OOCH,据此书写相应结构简式.
解答:
解:分子式为C7H7O2N的有机物分子结构中有一个苯环和互为对位的两个侧链,
甲既有酸性又有碱性,则A含有侧链为-NH2、-COOH,结构简式为 ;
;
乙只有酸性,则乙含有侧链为-OH、-CONH2,结构简式为: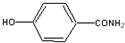 ;
;
丙既无酸性又无碱性,则丙中侧链为-CH3、-NO2,结构简式为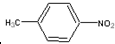 ;
;
丁只有碱性,则丁中侧链为-NH2、-OOCH,结构简式为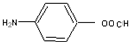 ,
,
故答案为: ;
; ;
; ;
; .
.
甲既有酸性又有碱性,则A含有侧链为-NH2、-COOH,结构简式为
 ;
;乙只有酸性,则乙含有侧链为-OH、-CONH2,结构简式为:
 ;
;丙既无酸性又无碱性,则丙中侧链为-CH3、-NO2,结构简式为
 ;
;丁只有碱性,则丁中侧链为-NH2、-OOCH,结构简式为
 ,
,故答案为:
 ;
; ;
; ;
; .
.
点评:本题考查有机物的推断、官能团结构与性质,注意利用题目信息及常见官能团的性质解答,题目难度中等.

练习册系列答案
 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案
相关题目
下列反应中可判断为可逆反应的是( )
| A、氢气和氯气点燃生成氯化氢,氯化氢受热分解为氢气和氯气 |
| B、氮气和氢气在高温、高压、催化剂作用下可以生成氨气,同时氨气又分解为氮气和氢气 |
| C、单质溴可以置换出碘,氯气又可以置换出溴 |
| D、氯气和水反应生成盐酸和次氯酸,次氯酸光照条件下可分解为盐酸和氧气 |
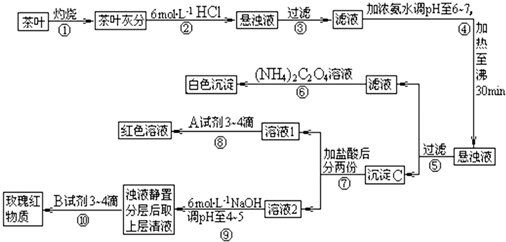
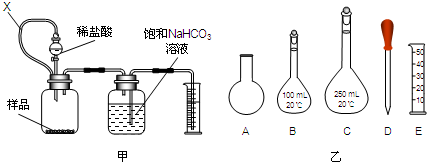
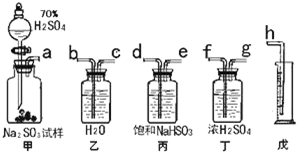 某研究性小组拟用下述方案测定一份亚硫酸钠试样的氧化变质程度.
某研究性小组拟用下述方案测定一份亚硫酸钠试样的氧化变质程度.