��Ŀ����
��ҵ����CuFeS2Ϊԭ��ұ��ͭ����Ҫ��ӦΪ��2CuFeS2��4O2 Cu2S��3SO2��2FeO(¯��)��
Cu2S��3SO2��2FeO(¯��)��
��2Cu2S��3O2 2Cu2O��2SO2����2Cu2O��Cu2S
2Cu2O��2SO2����2Cu2O��Cu2S 6Cu��SO2��������˵���������( )
6Cu��SO2��������˵���������( )
A����1 mol CuFeS2����1mol Cu��������2��75 molO2
B����ұ�������в����������к�����SO2���ɻ��������Ʊ�����
C���ڷ�Ӧ���У�Cu2S���������������ǻ�ԭ��
D���ڷ�Ӧ���У�SO2��������������ǻ�ԭ����
A
��������
���������A�����ݷ�Ӧ����ʽ��֪ÿ����6mol��Cu,������15mol��O2��������1 mol CuFeS2����1mol Cu��������2�� 5 molO2������B����ұ�������в����������к�����SO2����SO2����������SO3��Ȼ���SO3��Ũ�������վͿ�����ȡ���ᣬ��ȷ��C���ڷ�Ӧ���У�Cu2S�е�Cu���ϼ۽��ͣ��õ����ӣ�������������S���ϼ����ߣ�ʧȥ���ӣ�����ԭ�������Cu2S���������������ǻ�ԭ������ȷ��D���ڷ�Ӧ���У�SO2�������õ����ӵĻ�ԭ���Ҳ��CuFeS2�е�-2�۵�Sʧȥ���ӱ������õ��IJ�����SO2��������������ǻ�ԭ�����ȷ��
���㣺����������ԭ��Ӧ�еĵ���ת�ơ�������ʵ���;��֪ʶ��

��������ˮ�ķ�ĩ״������Ʒ�����ܺ���Al��Fe2O3��Cu2O��SiO2��Fe3O4�е�һ�ֻ��֣��о�С��ͨ��ʵ��ȷ����Ʒ�ijɷ֣�
����������֪���� Cu2O + 2H+ = Cu + Cu2+ + H2O��
�� ����������������Һ�г�����pH���±���
���� | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
��ʼ������pH | 1��8 | 6��3 | 5��2 |
��ȫ������pH | 3��0 | 8��3 | 6��7 |
��ע���������ӵ���ʼŨ��Ϊ0��1 mol��L-1
��ʵ�鲽�衿
��ȡһ������Ʒ���ձ��У�������NaOH��Һ����������������˵ù���A����ɫ��ҺB��
����B�м���ϡ���ᣬ���ְ�ɫ�����������μ�ϡ��������������ɫ������ȫ�ܽ⣻
����A�м�������ϡ���Ტ�ȣ�������ȫ�ܽ⣬����ҺC��
������C�м���NaClO��������Һ��pH��4��5���������ɫ���������˵õ�����ɫ��ҺD��
������D�м���NaOH��������Һ��pH��7��8��������ɫ��״������
��ش��������⣮
��1�����в�����������ӷ���ʽΪ ��
��2���ɢ�֪��ԭ��Ʒ��һ�������ڵ������� ��
��3����ҺC�г�H+��Cu2+��һ�������е��������� ��
��4�����м�NaClO��Ŀ���� ��
��5�������еõ�����ҺD��⣬�����ĵ缫��ӦʽΪ ������·����0��1mol����ͨ������������������������ g��
��6��������ʵ����Ի�ý��ۣ�ԭ��Ʒ���п��ܵijɷ����Ϊ���Ϊ
(�û�ѧʽ��ʾ)��
��10�֣�����ʯ����������������þ����Ҫ�������£�
��.��ȡ������þ������Һ��������ʯ��ۣ����ˣ����ڳ��³�ѹ�½ᾧ���Ƶô�����þ�����г���������Fe3+��Al3+��Fe2+���������ӣ�
��.�ᴿ������þ����������þ�������������ܽ⣬����������0.1mol/LH2O2��Һ���ٵ�����ҺpH��7~8���������ᴿ��
��.��ȡ������þ������II������Һ�м��������ˮ��
��֪�������������������������pH
Fe3+ | Al3+ | Fe2+ | Mg2+ | |
��ʼ����ʱ | 1.5 | 3.3 | 6.5 | 9.4 |
������ȫʱ | 3.7 | 5.2 | 9.7 | 12.4 |
��ش�
��1������II�м���������0.1mol/LH2O2��Һ��Ŀ���� �������ڵ�����ҺpH��7~8������Լ��� ������ĸ��ţ�
A.MgO B.Na2CO3 C������ˮ D.NaOH ��
��2����ҵ�ϳ���Mg2+��ת����Ϊ����ָ�꣬ȷ������III�Ʊ�������þ���չ��̵�����������
���У���Ӧ�¶���Mg2+ת���ʵĹ�ϵ��ͼ��ʾ��
�ٲ���III���Ʊ�������þ��Ӧ�����ӷ���ʽΪ ������ͼ����ʾ50��ǰ�¶���Mg2+ת����֮��Ĺ�ϵ�����жϴ˷�Ӧ�� ������ȡ����ȡ���Ӧ��

��ͼ�У��¶�������50������Mg2+ת�����½��Ŀ���ԭ���� ��
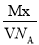 ��ʾ����( )
��ʾ����( )

