题目内容
13.a1、a2分别为A在甲、乙两个恒温容器中建立平衡体系A(g)?2B(g)时的转化率,已知甲容器保持压强不变,乙容器保持容器体积不变.在温度不变的情况下,均增加A的物质的量,下列判断正确的是( )| A. | a1、a2均减小 | B. | a1减小,a2增大 | C. | a1、不变,a2增大 | D. | a1不变,a2减小 |
分析 对于A(g)?2B(g),反应物和生成物都只有一种,如体积不变,增加A相当于增大压强,平衡逆向移动,如压强不变,平衡状态相同,为等效平衡,以此解答该题.
解答 解:对于A(g)?2B(g),反应物和生成物都只有一种,如体积不变,增加A相当于增大压强,平衡逆向移动A的转化率减小,
如压强不变,平衡状态相同,为等效平衡,则A的转化率不变,
故选D.
点评 本题考查平衡移动转化率的判断,为高频考点,侧重于学生的分析能力的考查,难度中等,本题采取虚拟条件转化,注意把握反应方程式的特征,题目难度不大.

练习册系列答案
 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目
4.用已知物质的量浓度的盐酸滴定未知物质的量浓度的NaOH溶液时,下列操作中不正确的是( )
| A. | 酸式滴定管用蒸馏水洗净后,直接加入已知物质的量浓度的盐酸 | |
| B. | 锥形瓶用蒸馏水洗净后,直接加入一定体积的未知物质的量浓度的NaOH溶液 | |
| C. | 滴定时,应左手控制活塞,右手摇动锥形瓶,眼睛时刻注视着锥形瓶内颜色的变化 | |
| D. | 读数时,视线与滴定管内液体的凹液面最低处保持一致 |
8.在密闭容器中反应aR(g)+bQ(g)?cX(g)+dY(g)达平衡后,保持温度不变,将容器体积增加一倍,达到新平衡时,X浓度是原来的60%,则下列说法正确的是( )
| A. | 平衡向正反应方向移动了 | B. | 物质R的转化率减少了 | ||
| C. | 物质X的质量分数减少了 | D. | a+b<c+d |
18.可逆反应2A(s)?C(g)+D(g)正向建立平衡后,维持其它条件不变,压缩容器的体积,下列说法正确的是( )
| A. | 正逆反应速率都增大 | |
| B. | 平衡不移动 | |
| C. | 再次平衡时c(D) 不变 | |
| D. | C的体积分数不再变化说明再次达到平衡 |
5.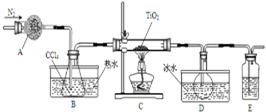 实验室利用反应TiO2(s)+CCl4(g)$\frac{\underline{\;\;△\;\;}}{\;}$TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4,实验装置示意图如下,有关物质性质如表.
实验室利用反应TiO2(s)+CCl4(g)$\frac{\underline{\;\;△\;\;}}{\;}$TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4,实验装置示意图如下,有关物质性质如表.
(1)仪器A的名称是干燥管,装置E中的试剂是浓硫酸.反应开始前依次进行如下操作:组装仪器、检验气密性、加装药品、通N2一段时间后点燃酒精灯.
(2)反应结束后的操作包括:a停止通N2 b熄灭酒精灯 c冷却至室温.正确的顺序为bca(填序号).选择这种顺序的理由是防止倒吸或避免生成的产物在受热情况下与氧气反应(二者任写其一均给分);欲分离D中的液态混合物,所采用操作的名称是蒸馏.
 实验室利用反应TiO2(s)+CCl4(g)$\frac{\underline{\;\;△\;\;}}{\;}$TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4,实验装置示意图如下,有关物质性质如表.
实验室利用反应TiO2(s)+CCl4(g)$\frac{\underline{\;\;△\;\;}}{\;}$TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4,实验装置示意图如下,有关物质性质如表.| 物质 | 熔点/℃ | 沸点/℃ | 其他 |
| CCl4 | -23 | 76 | 与TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产白雾 |
(2)反应结束后的操作包括:a停止通N2 b熄灭酒精灯 c冷却至室温.正确的顺序为bca(填序号).选择这种顺序的理由是防止倒吸或避免生成的产物在受热情况下与氧气反应(二者任写其一均给分);欲分离D中的液态混合物,所采用操作的名称是蒸馏.
2.在温度t1和t2(t2>t1)下,X2(g)和H2反应生成HX的平衡常数如下表:
下列说法不正确的是( )
| 化学方程式 | K(t1) | K(t2) | |
| ① | Br2 (g)+H2(g)?2HBr(g) | 5.6×107 | 9.3×106 |
| ② | I2 (g)+H2 (g)?2HI(g) | 43 | 34 |
| A. | ①和②均是放热反应 | |
| B. | 相同条件下,平衡体系中HX所占的比例:①>② | |
| C. | 其他条件不变时,增大压强可提高X2的平衡转化率 | |
| D. | 其他条件不变时,升高温度可加快HX的生成速率 |
3.石墨和金刚石都是碳元素的单质,石墨在一定条件下可转化为金刚石.已知12克石墨完全转化成金刚石时,要吸收EkJ的能量,下列说法正确的是( )
| A. | 石墨不如金刚石稳定 | |
| B. | 金刚石不如石墨稳定 | |
| C. | 金刚石和石墨的转化是物理变化 | |
| D. | C(s,金刚石)═C(s,石墨)△H=-1.9 kJ•mol-1 |
 某学校课外学习活动小组针对教材中铜与浓硫酸反应,提出了探究“能够与铜反应的硫酸的最低浓度是多少?”的问题,并设计了如下方案进行实验:
某学校课外学习活动小组针对教材中铜与浓硫酸反应,提出了探究“能够与铜反应的硫酸的最低浓度是多少?”的问题,并设计了如下方案进行实验: 某化学兴趣小组按如图所示装置探究铜与浓硫酸反应.随着温度的升高,有白雾产生,最终发现铜表面变黑,并有细小黑色颗粒物生成;试管B中有白色沉淀生成.
某化学兴趣小组按如图所示装置探究铜与浓硫酸反应.随着温度的升高,有白雾产生,最终发现铜表面变黑,并有细小黑色颗粒物生成;试管B中有白色沉淀生成.