题目内容
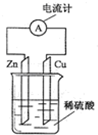 如图所示的原电池装置
如图所示的原电池装置(1)金属Zn组成的电极是
(2)金属Cu电极反应方程式为
(3)当导线上通过3.01×1022个电子时,锌片质量减少
考点:原电池和电解池的工作原理
专题:电化学专题
分析:(1)在用锌片、铜片和稀硫酸组成的原电池装置中,锌片的活泼性大于铜片的活泼性,所以锌片作负极,负极上锌失电子发生氧化反应;
(2)铜片作正极,正极上氢离子得电子发生还原反应;
(3)根据电极反应式,利用电子与反应物之间的关系求算.
(2)铜片作正极,正极上氢离子得电子发生还原反应;
(3)根据电极反应式,利用电子与反应物之间的关系求算.
解答:
解:(1)该装置中,活泼性较强的金属锌作负极,锌失电子发生氧化反应,电极反应式为:Zn-2e-═Zn2+;
故答案为:负;氧化;Zn-2e-═Zn2+;
(2)该装置中,活泼较弱的铜作正极,正极上氢离子得电子发生还原反应,电极反应式为:2H++2e-═H2↑;
故答案为:2H++2e-═H2↑;
(2)已知负极的电极反应式为Zn-2e-=Zn2+,当导线上通过3.01×1022个电子时,则电子的物质的量为0.05mol,则n(Zn)=0.025mol,所以锌片质量减少为:0.025mol×65g/mol=1.625g,金属Cu电极反应方程式为2H++2e-═H2↑,则Cu电极上生成的氢气为:n(H2)=0.025mol,
所以V(H2)=0.025mol×22.4L/mol=0.56L;
故答案为:1.625;0.56.
故答案为:负;氧化;Zn-2e-═Zn2+;
(2)该装置中,活泼较弱的铜作正极,正极上氢离子得电子发生还原反应,电极反应式为:2H++2e-═H2↑;
故答案为:2H++2e-═H2↑;
(2)已知负极的电极反应式为Zn-2e-=Zn2+,当导线上通过3.01×1022个电子时,则电子的物质的量为0.05mol,则n(Zn)=0.025mol,所以锌片质量减少为:0.025mol×65g/mol=1.625g,金属Cu电极反应方程式为2H++2e-═H2↑,则Cu电极上生成的氢气为:n(H2)=0.025mol,
所以V(H2)=0.025mol×22.4L/mol=0.56L;
故答案为:1.625;0.56.
点评:本题考查了原电池原理,主要涉及了电极的判断、电极方程式的书写、根据转移的电子求算有关物质等,侧重于基础知识的考查,题目难度不大.

练习册系列答案
相关题目
下列关于盐酸与醋酸两种稀溶液的说法正确的是( )
| A、相同浓度的两溶液中c(H+)相同 |
| B、100mL 0.1mol/L的两溶液能中和等物质的量的氢氧化钠 |
| C、pH=3的两溶液都稀释10倍,盐酸的pH大于醋酸的PH |
| D、两溶液中分别加人少量对应的钠盐,c(H+)均明显减小 |
约翰?芬恩等三位科学家在蛋白质等大分子研究领域的杰出贡献,获得了2002年的诺贝尔化学奖.下列有关说法正确的是( )
| A、蛋白质溶液中加入CuSO4溶液产生盐析现象 |
| B、蛋白质溶液不能产生丁达尔效应 |
| C、羊毛、棉花的主要成分都是蛋白质 |
| D、蛋白质在紫外线的照射下将会失去生理活性 |
已知反应I2(g)+H2(g)?2HI(g),该反应是放热反应,下列说法正确的是( )
| A、降低温度,正反应速率降低,逆反应速率升高 |
| B、使用催化剂将缩短达到平衡的时间 |
| C、达到平衡后,保持温度和容积不变,充入氩气,正、逆反应速率同等倍数增大 |
| D、达到平衡后,保持温度和压强不变,充入氩气,正、逆反应速率增加 |