题目内容
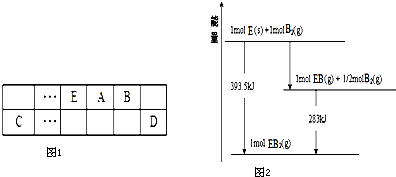
 已知A、B、C、D都是短周期元素,它们的原子半径大小为B>C>D>A.B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子有2个未成对电子.A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体.E是第四周期元素,其原子核外最外层电子数与A原子相同,其余各层电子均充满.回答下列问题(用元素符号或化学式表示).
已知A、B、C、D都是短周期元素,它们的原子半径大小为B>C>D>A.B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子有2个未成对电子.A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体.E是第四周期元素,其原子核外最外层电子数与A原子相同,其余各层电子均充满.回答下列问题(用元素符号或化学式表示).(1)M分子中B原子轨道的杂化类型为
(2)化合物CA3的沸点比化合物BA4的高,其主要原因是
(3)写出与BD2互为等电子体的C3-的结构式
(4)E+的核外电子排布式为
(5)向E的硫酸盐溶液中通入过量的CA3,可生成[E(CA3)4]2+配离子,1mol[E(CA3)4]2+中含有σ键的数目为
考点:位置结构性质的相互关系应用,配合物的成键情况,晶胞的计算
专题:元素周期律与元素周期表专题,化学键与晶体结构
分析:A、B、C、D都是短周期元素,它们的原子半径大小为B>C>D>A,B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同,则B是C元素;D原子有2个未成对电子,且D原子半径小于B,则D是O元素;C的原子半径小于B而大于D,则C是N元素;A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,则该气体是甲醛,所以A是H元素;E是第四周期元素,其原子核外最外层电子数与A原子相同,其余各层电子均充满,则E是铜元素,据此解答.
解答:
解:A、B、C、D都是短周期元素,它们的原子半径大小为B>C>D>A,B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同,则B是C元素;D原子有2个未成对电子,且D原子半径小于B,则D是O元素;C的原子半径小于B而大于D,则C是N元素;A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,则该气体是甲醛,所以A是H元素;E是第四周期元素,其原子核外最外层电子数与A原子相同,其余各层电子均充满,则E是铜元素,
(1)M为HCHO,分子中C原子成3个σ键,没有孤电子对,杂化轨道数目为3,则C原子采取sp2杂化,
故答案为:sp2;
(2)NH3分子间能形成氢键,沸点高于CH3,
故答案为:NH3分子间能形成氢键;
(3)与CO2互为等电子体的N3-,二者结构式相似,故N3-结构式为[N=N=N]-,
故答案为:[N=N=N]-;
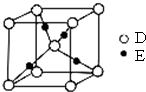
(4)Cu+的核外电子排布式为 1s22s22p63s23p63d10,由晶胞结构可知,E形成的阳离子位于晶胞内部,该晶体1个晶胞中阳离子的个数为4,
故答案为:1s22s22p63s23p63d10;4;
(5)向硫酸铜溶液中通入过量的NH3,可生成[Cu(NH3)4]2+配离子,N-H键为σ键,配位键属于σ键,故1mol[Cu(NH3)4]2+中含有16molσ键,含有σ键的数目为 16×6.02×1023,
故答案为:16×6.02×1023.
(1)M为HCHO,分子中C原子成3个σ键,没有孤电子对,杂化轨道数目为3,则C原子采取sp2杂化,
故答案为:sp2;
(2)NH3分子间能形成氢键,沸点高于CH3,
故答案为:NH3分子间能形成氢键;
(3)与CO2互为等电子体的N3-,二者结构式相似,故N3-结构式为[N=N=N]-,
故答案为:[N=N=N]-;
(4)Cu+的核外电子排布式为 1s22s22p63s23p63d10,由晶胞结构可知,E形成的阳离子位于晶胞内部,该晶体1个晶胞中阳离子的个数为4,
故答案为:1s22s22p63s23p63d10;4;
(5)向硫酸铜溶液中通入过量的NH3,可生成[Cu(NH3)4]2+配离子,N-H键为σ键,配位键属于σ键,故1mol[Cu(NH3)4]2+中含有16molσ键,含有σ键的数目为 16×6.02×1023,
故答案为:16×6.02×1023.
点评:本题是对物质结构的考查,涉及杂化轨道、氢键、等电子体、晶胞结构、核外电子排布、配合物、化学键等知识点,需要学生具备扎实的基础与灵活应用能力,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
元素R、X、T、Z、Q在元素周期表中的相对位置如表所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( )
| R | ||
| X | T | Z |
| Q |
| A、非金属性:Z<T<X |
| B、R与Q的电子数相差26 |
| C、气态氢化物稳定性:R<T<Q |
| D、最高价氧化物的水化物的酸性:T<Q |
已知下面三个数据:7.2×10-4、4.6×10-4、4.9×10-10分别是下列有关的三种酸的电离常数,若已知下列反应可以发生:NaCN+HNO2→HCN+NaNO2 NaCN+HF→HCN+NaF NaNO2+HF→HNO2+NaF,由此可判断下列叙述不正确的是( )
| A、K(HF)=7.2×10-4 |
| B、K(HNO2)=4.9×10-10 |
| C、必须根据其中三个反应才可得出结论 |
| D、K(HCN)<K(HNO2)<K(HF) |
下列化学方程式(含相关条件)与实际化工生产功能相符合的是( )
A、工业上最重要的“人工固氮”反应:N2+3H2
| |||
B、工业法合成盐酸:H2+Cl2
| |||
C、工业上获取NaCl:2Na+Cl2
| |||
D、氯碱工业:2NaCl+2H2O
|
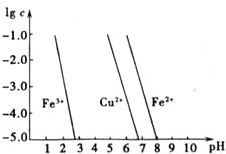 如图横坐标为溶液pH,纵坐标为金属离子物质的量浓度的对数值(当溶液中金属离子浓度≤10-5mol?L-1时,可认为沉淀完全),试回答:
如图横坐标为溶液pH,纵坐标为金属离子物质的量浓度的对数值(当溶液中金属离子浓度≤10-5mol?L-1时,可认为沉淀完全),试回答: