题目内容
9.下列选项括号中的物质是除去杂质所需要的药品,其中错误的是( )| A. | NaCl中含有杂质Na2SO4(适量氯化钡) | |
| B. | FeSO4 中含有杂质CuSO4(铁粉) | |
| C. | SO2中含有少量HCl气体(氢氧化钠溶液) | |
| D. | CO2中含有少量的CO(灼热的氧化铜) |
分析 A.硫酸钠与氯化钡反应生成硫酸钡和氯化钠;
B.Fe与硫酸铜反应生成硫酸亚铁和Cu;
C.二者均与NaOH溶液反应;
D.CO还原CuO反应生成二氧化碳.
解答 解:A.硫酸钠与氯化钡反应生成硫酸钡和氯化钠,则反应后过滤可分离,故A正确;
B.Fe与硫酸铜反应生成硫酸亚铁和Cu,则反应后过滤可分离,故B正确;
C.二者均与NaOH溶液反应,不能除杂,应选饱和亚硫酸氢钠溶液,故C错误;
D.CO还原CuO反应生成二氧化碳,则利用灼热的氧化铜可除杂,故D正确;
故选C.
点评 本题考查混合物分离提纯的综合应用,为高频考点,把握物质的性质、性质差异及发生的反应等为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
20. 以下元素均为短周期元素:
以下元素均为短周期元素:
(1)B在周期表中的位置第二周期第 VIA族,C离子的结构示意图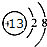 .
.
(2)D的最低价含氧酸的电子式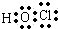 .
.
(3)M的简单气态氢化物与B的单质形成燃料电池(KOH为电解液),写出其负极反应方程式2NH3-6e-+6OH-═N2+6H2O.
(4)A在真空高压下能与由D、E组成的分子呈正四面体结构的化合物Y反应生成2种固体物质,其中一种是自然界中硬度最大的物质.该反应的化学方程式:4Na+CCl4$\frac{\underline{\;真空高压\;}}{\;}$4NaCl+C;
(5)仅由A、B、E组成的一种生活中的常用盐,其中A的质量分数为43%,其水溶液与D单质物质的量比为1:1反应的离子方程式为CO32-+Cl2+H2O=ClO-+Cl-+HCO-3.
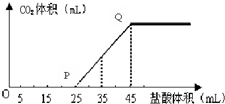
(6)A的最高价氧化物的水化物的溶液中通入一定量CO2得溶液X,X中逐滴加入1mol•L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如图所示:
①X溶液中溶质的化学式NaOH和Na2CO3.
②当加入35mL盐酸时,产生CO2的体积为224mL(标准状况).
 以下元素均为短周期元素:
以下元素均为短周期元素:| 元素代号 | 相关信息 |
| M | 非金属元素,其气态氢化物的水溶液呈碱性 |
| A | A的单质与冷水剧烈反应,得到强碱性溶液 |
| B | B的原子最外层电子数是 内层电子数的三倍 |
| C | 在第三周期中,C的简单离子半径最小 |
| D | A、B、D组成的36电子的化合物X是家用消毒剂的主要成分 |
| E | 所有有机物中都含有E元素 |
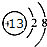 .
.(2)D的最低价含氧酸的电子式
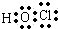 .
.(3)M的简单气态氢化物与B的单质形成燃料电池(KOH为电解液),写出其负极反应方程式2NH3-6e-+6OH-═N2+6H2O.
(4)A在真空高压下能与由D、E组成的分子呈正四面体结构的化合物Y反应生成2种固体物质,其中一种是自然界中硬度最大的物质.该反应的化学方程式:4Na+CCl4$\frac{\underline{\;真空高压\;}}{\;}$4NaCl+C;
(5)仅由A、B、E组成的一种生活中的常用盐,其中A的质量分数为43%,其水溶液与D单质物质的量比为1:1反应的离子方程式为CO32-+Cl2+H2O=ClO-+Cl-+HCO-3.
(6)A的最高价氧化物的水化物的溶液中通入一定量CO2得溶液X,X中逐滴加入1mol•L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如图所示:
①X溶液中溶质的化学式NaOH和Na2CO3.
②当加入35mL盐酸时,产生CO2的体积为224mL(标准状况).
4.化学与环境、工农业生产等密切相关,下列叙述正确的是( )
| A. | 光化学烟雾与大量排放碳氢化合物和氮氧化合物有关 | |
| B. | 将草木灰和硫酸铵混合施用,肥效更高 | |
| C. | 棉花的主要成分是纤维素,石英玻璃、陶瓷和水泥均属于硅酸盐产品 | |
| D. | 硫酸工业尾气未经处理就直接排放,将直接导致“温室效应” |
18.我国科学家合成镅的一种新同位素23595Am,与铀23592U比较,下列叙述中正确的是( )
| A. | 它们互为同位素 | B. | 原子核中的中子数相同 | ||
| C. | 具有相同的质子数 | D. | 23595Am比23592U少3个中子 |
 .
. .
.