题目内容
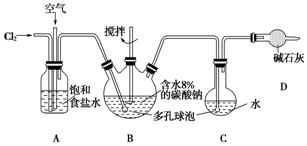
7.实验室以一种工业废渣(含80%~90%的Ca(OH)2,其余为焦炭等不溶物)为原料制备KClO3的实验过程如图1:几种物质的溶解度如图2:
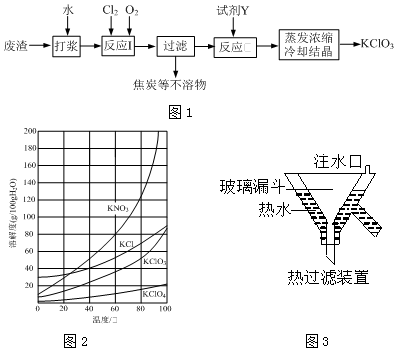
(1)反应I的目的是制备Ca(ClO3)2,写出该反应的化学方程式:2Ca(OH)2+2Cl2+5O2=2Ca(ClO3)2+2H2O;在通入Cl2和O2比例、废渣量均一定的条件下,为使Cl2转化完全,可采取的合理措施是缓慢通入Cl2、O2(搅拌浆料或控制合适的温度).
(2)若过滤时滤液出现浑浊,其可能的原因是AB(填序号).
A.漏斗中液面高于滤纸边缘 B.滤纸已破损 C.滤纸未紧贴漏斗内壁
(3)所加试剂Y选用KCl而不用KNO3的原因是防止产物KClO3中含有较多的KNO3杂质.
(4)已知:4KClO3$\frac{\underline{\;400℃\;}}{\;}$3KClO4+KCl;2KClO3$\frac{\underline{\;600℃\;}}{\;}$2KCl+3O2↑.实验室可用KClO3制备高纯KClO4固体,实验中必须使用的用品有:热过滤装置(如图3所示)、冰水.
①热过滤装置中玻璃漏斗的下端露出热水浴部分不宜过长,其原因是防止滤液冷却析出的晶体堵塞漏斗.
②请补充完整由KClO3制备高纯KClO4固体的实验方案:
向坩埚中加入一定量的KClO3,控制温度400℃,使KClO3充分分解,将所得固体溶于水并煮沸至有大量固体析出,用热过滤装置过滤,并用冰水洗涤滤渣2~3次,在低温下干燥得KClO4固体.
分析 工业废渣(含80%~90%的Ca(OH)2,其余为焦炭等不溶物),加入水打浆,通入氯气氯化和氢氧化钙反应在80℃生成氯酸钙和水,过滤掉焦炭等不溶物,向滤液中加入饱和KCl溶液,转化为KClO3的溶液,蒸发浓缩,冷却结晶,趁热过滤得到析出KClO3的晶体,据此分析作答.
解答 解:(1)反应I的目的是制备Ca(ClO3)2,发生的反应化学方程式为:2Ca(OH)2+2Cl2+5O2=2Ca(ClO3)2+2H2O;为使Cl2转化完全,可缓慢通入Cl2、O2(搅拌浆料或控制合适的温度);
故答案为:2Ca(OH)2+2Cl2+5O2=2Ca(ClO3)2+2H2O;缓慢通入Cl2、O2(搅拌浆料或控制合适的温度);
(2)若过滤时滤液出现浑浊,其可能的原因是:漏斗中液面高于滤纸边缘、滤纸已破损;
故答案为:AB;
(3)KNO3的溶解度随温度的升高而增大,防止产物KClO3中含有较多的KNO3杂质,所加试剂Y选用KCl而不用KNO3;
故答案为:防止产物KClO3中含有较多的KNO3杂质;
(4)①为防止滤液冷却析出的晶体堵塞漏斗,热过滤装置中玻璃漏斗的下端露出热水浴部分不宜过长;
故答案为:防止滤液冷却析出的晶体堵塞漏斗;
②已知:4KClO3$\frac{\underline{\;400℃\;}}{\;}$3KClO4+KCl,由KClO3制备高纯KClO4固体的实验方案:向坩埚中加入一定量的KClO3,控制温度400℃,使KClO3充分分解,将所得固体溶于水并煮沸至有大量固体析出,用热过滤装置过滤,并用冰水洗涤滤渣2~3次,在低温下干燥得KClO4固体;
故答案为:控制温度400℃,使KClO3充分分解,将所得固体溶于水并煮沸至有大量固体析出,用热过滤装置过滤,并用冰水洗涤滤渣2~3次.
点评 本题考查了物质的制备和分离提纯的过程分析判断,实验条件和物质性质的理解应用,实验设计和反应流程、原理理解是关键,题目难度中等.

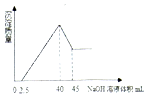 取一定量的铝土矿(含Al2O3、Fe2O3、SiO2)样品,放入盛有200mL H2SO4溶液的烧杯中,充分反应后过滤,向滤液中加入10mol/L的NaOH溶液,产生沉淀的量与所加NaOH溶液的体积的关系如图所示.则原H2SO4物质的量浓度是( )
取一定量的铝土矿(含Al2O3、Fe2O3、SiO2)样品,放入盛有200mL H2SO4溶液的烧杯中,充分反应后过滤,向滤液中加入10mol/L的NaOH溶液,产生沉淀的量与所加NaOH溶液的体积的关系如图所示.则原H2SO4物质的量浓度是( )| A. | 1mol/L | B. | 2mol/L | C. | 3mol/L | D. | 4mol/L |
| A. | 2:1:2:1 | B. | 1:2:1:2 | C. | 4:2:2:1 | D. | 1:2:2:1 |
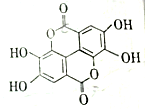 二缩双是一种广泛存在于各种软果、坚果等植物组织中的天然组分,其结构简式如图,二缩双在稀硫酸作用下水解不能得到的产物的类别是( )
二缩双是一种广泛存在于各种软果、坚果等植物组织中的天然组分,其结构简式如图,二缩双在稀硫酸作用下水解不能得到的产物的类别是( )| A. | 酚 | B. | 醛 | C. | 芳香族化合物 | D. | 羧酸 |
(1)若因为反应中有放热现象,而造成少量HCl在反应中挥发,则测得的中和热偏小(填“偏大”“偏小”或“不变”).
(2)该实验小组做了三次实验,每次取溶液各50mL,并记录如表原始数据.
| 实验 序号 | 起始温度t1/℃ | 终止温度 (t2)/℃ | 温差 (t2-t1)/℃ | ||
| 盐酸 | NaOH溶液 | 平均值 | |||
| 1 | 25.1 | 24.9 | 25.0 | 31.6 | 6.6 |
| 2 | 25.1 | 25.1 | 25.1 | 31.8 | 6.7 |
| 3 | 25.1 | 25.1 | 25.1 | 31.9 | 6.8 |
(3)若用等浓度的醋酸与NaOH溶液反应,则测得的中和热的数值会偏小(填“偏大”“偏小”或“不变”),其原因是醋酸为弱酸,电离过程为吸热过程.
(4)在中和热测定实验中存在用水洗涤温度计上的盐酸溶液的步骤,若无此操作步骤,则测得的中和热的数值偏小(填“偏大”“偏小”或“不变”).
已知101kPa、25℃时,1mol下列物质完全燃烧生成稳定状态化合物时放出的热量数据如表:
| 物质 | 氢气 | 原煤 (主要成份是C) | 汽油 (主要成份C8H18) |
| 热量(kJ) | 285.8 | 250.9 | 4910 |
(2)工业上电解饱和盐水的副产物之一是H2,反应的离子方程式是2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑.
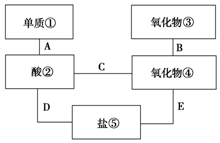 现有稀硫酸、纯碱、二氧化碳、铜片、食盐、生石灰、铁片和木炭粉8种物质.
现有稀硫酸、纯碱、二氧化碳、铜片、食盐、生石灰、铁片和木炭粉8种物质.