题目内容
19.请你利用实验室的固体氯化钠试剂,配制500mL 0.4mol/L 的NaCl溶液?(需要哪些仪器、操作步骤如何)分析 用固体配制一定物质的量浓度溶液一般步骤:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶、贴标签,据此选择需要的仪器及正确操作步骤.
解答 解:利用实验室的固体氯化钠试剂,配制500mL 0.4mol/L 的NaCl溶液,首先需要计算所需固体氯化钠的质量:m(NaCl)=0.5L×0.4mol/L×58.5g/mol=11.7g,然后用托盘天平称量固体氯化钠11.7g,将氯化钠在烧杯中溶解,用玻璃棒不断搅拌,冷却后,将氯化钠溶液用玻璃棒引流转移入容量瓶中,洗涤烧杯和玻璃棒两次,洗涤液一并转入容量瓶中,振荡,然后直接向容量瓶中加水到液面接近刻度1~2cm处;改用胶头滴管加水到瓶颈刻度处,使溶液凹液面正好与刻度线相切,把容量瓶塞好,上下颠倒,反复摇匀,装入干燥的试剂瓶中,贴上标签,注明名称、浓度、体积,用到的仪器依次为:托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管;
故答案为:托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管;
步骤为:
①计算:所需固体氯化钠的质量:m(NaCl)=0.5L×0.4mol/L×58.5g/mol=11.7g.
②用托盘天平称取固体氯化钠11.7g.
③将固体氯化钠放入烧杯中,并加入少量的蒸馏水用玻璃棒搅拌使之溶解.
④将氯化钠溶液用玻璃棒引流转移入容量瓶中.
⑤洗涤烧杯和玻璃棒两次,洗涤液一并转入容量瓶中,振荡.
⑥然后直接向容量瓶中加水到液面接近刻度1~2cm处;改用胶头滴管加水到瓶颈刻度处,使溶液凹液面正好与刻度线相切.
⑦把容量瓶塞好,上下颠倒,反复摇匀.
⑧装入干燥的试剂瓶中,贴上标签,注明名称、浓度、体积.
点评 本题考查了一定物质的量浓度溶液的配制,明确配制原理是解题关键,注意操作步骤及仪器的选择.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
10.已知Ksp(AgCl)=1.56×10-10,Ksp(Ag2CO3)=8.45×10-12,Ksp(AgBr)=7.7×10-13.某溶液中含有Cl-、CO32-和Br-浓度均为0.010mol•L-1,向该溶液中逐滴加入0.010mol•L-1的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为( )
| A. | Cl-、Br-、CO32- | B. | Br-、CO32-、Cl- | C. | CO32-、Br-、Cl- | D. | Br-、Cl-、CO32- |
9.在水电离出来的c(H+)=10-13mol/L的溶液中一定不能大量共存的离子组是( )
| A. | NH4+、Cu2+、Cl-、NO3- | B. | K+、Na+、SO32-、S2- | ||
| C. | K+、Na+、AlO2-、SO42- | D. | Ba2+、Fe2+、NO3-、Br- |
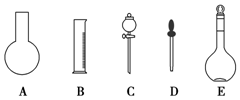 实验室需要0.1mol•L-1 NaOH溶液450mL和0.5mol•L-1硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题:
实验室需要0.1mol•L-1 NaOH溶液450mL和0.5mol•L-1硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题: ;.
;.
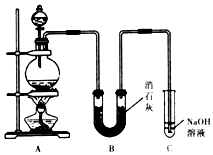 某学生设计如图所示的实验装置,利用氯气与潮湿的消石灰反应制取漂白粉,据此回答下列问题:
某学生设计如图所示的实验装置,利用氯气与潮湿的消石灰反应制取漂白粉,据此回答下列问题: MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O CaCl2+Ca(ClO)2+2H2O
CaCl2+Ca(ClO)2+2H2O