题目内容
11.下列过程或现象与盐类水解无关的是( )| A. | 纯碱溶液去油污 | B. | 铁在潮湿的环境下生锈 | ||
| C. | 加热氯化铁溶液颜色变深 | D. | 浓硫化钠溶液有臭鸡蛋味 |
分析 A.纯碱为强碱弱酸盐,水解呈碱性;
B.铁易发生电化学腐蚀;
C.氯化铁为强酸弱碱盐,加热促进水解;
D.硫化钠溶液中硫离子水解生成少量硫化氢气体有臭鸡蛋气味.
解答 解:A.纯碱为强碱弱酸盐,水解呈碱性,可使油污在碱性条件下水解而除去,与盐类的水解有关,故A不选;
B.铁易发生电化学腐蚀,与盐类的水解无关,故B选;
C.氯化铁为强酸弱碱盐,加热促进水解生成氢氧化铁,溶液颜色变深,故C不选;
D.溶液有臭味是因为硫化钠水解后产生了少量的硫化氢,与水解有关,故D不选.
故选B.
点评 本题考查盐类水解的应用,侧重于化学知识的综合运用的考查,注意把握盐类水解的原理,题目难度不大.

练习册系列答案
相关题目
6.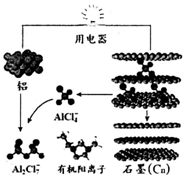 2015年中美专家研制出可在一分钟内完成充电的超常性能铝离子电池,该电池以金属铝和石墨为电极,用AlCl4-、A12C17-和有机阳离子组成电解质溶液,其放电工作原理如图所示.下列说法不正确的是( )
2015年中美专家研制出可在一分钟内完成充电的超常性能铝离子电池,该电池以金属铝和石墨为电极,用AlCl4-、A12C17-和有机阳离子组成电解质溶液,其放电工作原理如图所示.下列说法不正确的是( )
 2015年中美专家研制出可在一分钟内完成充电的超常性能铝离子电池,该电池以金属铝和石墨为电极,用AlCl4-、A12C17-和有机阳离子组成电解质溶液,其放电工作原理如图所示.下列说法不正确的是( )
2015年中美专家研制出可在一分钟内完成充电的超常性能铝离子电池,该电池以金属铝和石墨为电极,用AlCl4-、A12C17-和有机阳离子组成电解质溶液,其放电工作原理如图所示.下列说法不正确的是( )| A. | 放电时,电子山石墨电极经用电器流向铝电极 | |
| B. | 充电时,铝电极上发生氧化反应 | |
| C. | 充电时,AlCI4-向铝电极方向移动 | |
| D. | 放电时,负极反应为:Al-3e-+7 AlCl4-═4A12C17- |
2.N2和CH4组成的混合气体,相同条件下其相对于H2的密度为12,则混合气体中N2和CH4的体积比为( )
| A. | 1:1 | B. | 4:1 | C. | 1:4 | D. | 8:7 |
6.某澄清溶液可能由KI、NaNO3、CaCl2和Na2CO3中的一种或几种混合而成,为鉴定其组成,依次进行如下实验;(1)上述溶液中滴加AgNO3溶液有浅黄色沉淀产生;(2)将沉淀滤出加HNO3时,沉淀部分溶解,有气体放出;(3)向一份溶液中加淀粉溶液,再加适量氯水,溶液显蓝色.根据以上实验可判断( )
| A. | 一定有CaCl2和Na2CO3,一定没有KI,可能有NaNO3 | |
| B. | 一定有KI、Na2CO3,可能有NaNO3、CaCl2 | |
| C. | 一定有KI、Na2CO3,可能有NaNO3,一定没有CaCl2 | |
| D. | 只有Na2CO3,可能有NaNO3,一定没有KI、CaCl2 |
16.下列事实一定能说明HF是弱酸的是( )
| A. | 用HF溶液做导电性实验,灯泡很暗 | |
| B. | HF与水能以任意比混溶 | |
| C. | 1mol/L的HF水溶液能使紫色石蕊试液变红 | |
| D. | 常温下NaF溶液的pH大于7 |
20.下列有关说法正确的是( )
| A. | CaCO3(s)=CaO(s)+CO2(g)室温下不能自发进行,说明该反应的△S<0 | |
| B. | 镀铜铁制品镀层受损后,铁制品比受损前更容易生锈 | |
| C. | N2(g)+3H2(g)?2NH3(g)△H<0,其他条件不变时升高温度,氢气的反应速率和转化率均增大 | |
| D. | 水的离子积常数Kw随着温度的升高而增大,说明水的电离是放热反应 |
1.下列离子方程式书写正确的是( )
| A. | 硫酸亚铁溶液中加入用琉酸酸化的过氧化氢溶液:Fe2++2H++H2O2═Fe3++2H2O | |
| B. | 向 AlCl3溶液中加入过量的氨水:Al3++4NH4•H2O═AlO2-+4NH4++2H2O | |
| C. | 用惰性电极电解 MgCl2溶液:2Cr+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- | |
| D. | 向 NaOH 溶液中滴加过量Ca(HCO3)2 溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O |


 .写出该反应的离子方程式Fe3S4+6H+=3H2S↑+3Fe2++S.
.写出该反应的离子方程式Fe3S4+6H+=3H2S↑+3Fe2++S.