题目内容
5.今有FeS和FeBr2混合物,其中Fe元素的质量分数为56%,则溴元素的质量分数为( )| A. | 20% | B. | 15% | C. | 12% | D. | 10% |
分析 FeS和FeBr2混合物,假设平均分子式为FeSxBry,根据化合价代数和为0与Fe元素质量分数联立计算x、y的值,进而计算溴元素质量分数.
解答 解:FeS和FeBr2混合物,假设平均分子式为FeSxBry,
根据化合价代数和为0,则:2x+y=2,
根据Fe元素质量分数为56%,则32x+80y+56=100,
联立解得x=$\frac{29}{32}$,y=$\frac{3}{16}$
故溴元素质量分数为$\frac{80×\frac{3}{16}}{100}$=15%,
故选B.
点评 本题考查混合物中元素质量分数计算,利用平均分子式简化计算,侧重考查学生分析计算能力,难度中等.

练习册系列答案
相关题目
15.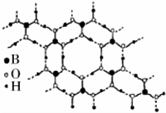 正硼酸(H3B03)是一种片层状结构的白色晶体,层内的H3BO3分子通过氢键相连(层状结构如图所示,图中“虚线”表示氢键).下列有关说法正确的是( )
正硼酸(H3B03)是一种片层状结构的白色晶体,层内的H3BO3分子通过氢键相连(层状结构如图所示,图中“虚线”表示氢键).下列有关说法正确的是( )
 正硼酸(H3B03)是一种片层状结构的白色晶体,层内的H3BO3分子通过氢键相连(层状结构如图所示,图中“虚线”表示氢键).下列有关说法正确的是( )
正硼酸(H3B03)是一种片层状结构的白色晶体,层内的H3BO3分子通过氢键相连(层状结构如图所示,图中“虚线”表示氢键).下列有关说法正确的是( )| A. | H3BO3分子的稳定性与氢键有关 | |
| B. | 含1mol H3BO3的晶体中有3mol氢键 | |
| C. | 分子中B、O最外层为8e-稳定结构 | |
| D. | 同层分子间的主要作用力是范德华力 |
16.下列设计的实验方案能达到实验目的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 证明其他条件不变时,增大反应物浓度,反应速率加快 | 常温下,对比等量铝粉分别与稀硫酸反应的反应速率 |
| B | 证明SO2具有氧化性 | 将SO2通入酸性KMnO4溶液中,观察溶液是否褪色 |
| C | 证明Ksp(AgCl)>Ksp(Ag2S) | 向2mL0.1mol•L-1AgNO3溶液中加入1mL0.1mol•L-1NaCl溶液,出现白色沉淀,再加入几滴0.1mol•L-1的Na2S溶液,有黑色沉淀生成 |
| D | 证明“84”消毒液(含NaClO)的氧化能力随溶液pH减小而增强 | 将“84”消毒液滴入品红溶液中,褪色缓慢,若同时加入食醋,红色很快退去 |
| A. | A | B. | B | C. | C | D. | D |
13.如图为立方烷的结构简式,其二氯代物有( )
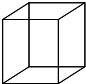

| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
20.下列各组离子在溶液中能大量共存的是( )
| A. | H+、Na+、Fe2+、NO3- | B. | Fe3+、Fe2+、SO42-、NO3- | ||
| C. | Na+、OH-、SO42-、H2PO4- | D. | Al3+、Na+、S2-、SO42- |
10.Mg-AgCl电池是一种以海水为电解质溶液的水激活电池.下列叙述错误的是( )
| A. | 负极反应式为Mg-2e-=Mg2+ | |
| B. | 正极反应式为Ag++e-=Ag | |
| C. | 电池放电时Cl-由正极向负极迁移 | |
| D. | 负极会发生副反应Mg+2H2O=Mg(OH)2+H2↑ |
17.三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室.下列叙述正确的是( )
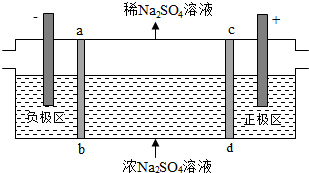

| A. | 通电后中间隔室的SO42-离子向正极迁移,正极区溶液pH增大 | |
| B. | 该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品 | |
| C. | 负极反应为2H2O-4e-=O2+4H+,负极区溶液pH降低 | |
| D. | 当电路中通过1mol电子的电量时,会有0.5mol的O2生成 |
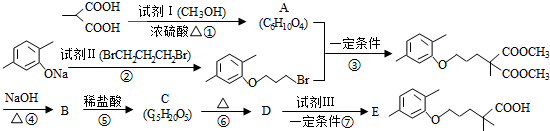
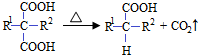 (R1和R2代表烷基)
(R1和R2代表烷基)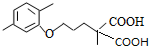 $\stackrel{加热}{→}$
$\stackrel{加热}{→}$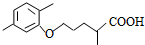 +CO2↑.
+CO2↑.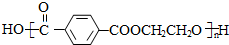 .
.