题目内容
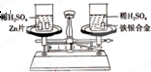 如图所示,在托盘天平的左右两托盘中各放置一只烧杯,调节天平使之平衡,向烧杯中分别注入足量且等质量、等浓度的稀硫酸,然后向两只烧杯中分别加入相同质量的锌片和铁银合金,反应完成后,天平仍保持平衡.合金中铁和银的质量比为( )
如图所示,在托盘天平的左右两托盘中各放置一只烧杯,调节天平使之平衡,向烧杯中分别注入足量且等质量、等浓度的稀硫酸,然后向两只烧杯中分别加入相同质量的锌片和铁银合金,反应完成后,天平仍保持平衡.合金中铁和银的质量比为( )| A、65:56 | B、56:108 |
| C、56:9 | D、65:9 |
考点:有关混合物反应的计算,计量仪器及使用方法
专题:计算题
分析:反应后天平仍然平衡,则反应生成氢气的质量相等,设生成氢气的质量为2g,反应消耗锌的质量为x、消耗铁的质量为y,根据反应方程式计算出x、y,再根据反应前金属质量相等计算出银的质量,从而可计算出合金中铁和银的质量比.
解答:
解:设产生氢气的质量为2g,需要锌的质量为x,需要Fe的质量为y,则有:
Zn+H2SO4═ZnSO4+H2↑
65 2
x 2g
=
,
x=65g,
Fe+H2SO4═FeSO4+H2↑
56 2
y 2g
=
y=56g,
锌片和铁银合金的质量相等,故银的质量为:65g-56g=9g,
所以合金中铁和银的质量比为56g:9g=56:9,
故选C.
Zn+H2SO4═ZnSO4+H2↑
65 2
x 2g
| 65 |
| x |
| 2 |
| 2 |
x=65g,
Fe+H2SO4═FeSO4+H2↑
56 2
y 2g
| 56 |
| y |
| 2 |
| 2 |
y=56g,
锌片和铁银合金的质量相等,故银的质量为:65g-56g=9g,
所以合金中铁和银的质量比为56g:9g=56:9,
故选C.
点评:本题考查了有关混合物反应计算,题目难度中等,明确题干信息及反应原理为解答关键,试题侧重考查学生的分析、理解能力及化学计算能力.

练习册系列答案
相关题目
无色透明溶液中能大量共存的离子组是( )
| A、Na+、Al3+、HCO3-、NO3- |
| B、AlO2-、Cl-、Mg2+、K+ |
| C、NH4+、Na+、CH3COO-、NO3- |
| D、Na+、NO3-、ClO-、I- |
海水中提取的食盐经精制(除去Ca2+、Mg2+和SO42-)后,含有少量的氯化钾等杂质,为了提纯并得到更多的食盐,用某液体洗涤,该液体最好是( )
| A、蒸馏水 |
| B、饱和食盐水 |
| C、饱和氯化钾溶液 |
| D、75%的酒精溶液 |
常温下,下列有关醋酸的叙述中不正确的是( )
| A、pH=5.6的由CH3COOH与CH3COONa组成的混合溶液中:c(Na+)<c(CH3C00-) |
| B、将pH=a的醋酸稀释为pH=a+1的过程中,c(OH-)不断增大 |
| C、等体积pH=a的醋酸与pH=b的NaOH溶液恰好中和时,a+b=14 |
| D、浓度均为o.1 mol-1的CH3COOH溶液和氨水等体积混合后:c(CH3COO-)+c(OH-)=c(H+)+c(NH4+) |
木炭屑与浓HNO3共热,产生的气体等分为①和②两份,将第一份气体先导入适量蒸馏水中再导入石灰水中,将第二份气体直接导入石灰水中,则石灰水的变化可能是( )
| A、①不变浑浊②变乳白色 |
| B、①变乳白色②不变浑浊 |
| C、①变乳白色②变乳白色 |
| D、不变浑浊②变浅黄色 |