题目内容
在t℃时,将0.2 mol X和0.8 mol Y充入体积恒定的密闭容器中,当反应X(g)+Y(g) 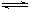 nZ(g)+R(g)达到平衡时,若将反应混合气体中各物质浓度均增大一倍,X的转化率不变,已知t℃时该反应的K=1,则X的转化率为
nZ(g)+R(g)达到平衡时,若将反应混合气体中各物质浓度均增大一倍,X的转化率不变,已知t℃时该反应的K=1,则X的转化率为
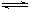 nZ(g)+R(g)达到平衡时,若将反应混合气体中各物质浓度均增大一倍,X的转化率不变,已知t℃时该反应的K=1,则X的转化率为
nZ(g)+R(g)达到平衡时,若将反应混合气体中各物质浓度均增大一倍,X的转化率不变,已知t℃时该反应的K=1,则X的转化率为| A.80% | B.65% | C.45% | D.37% |
A
略

练习册系列答案
相关题目
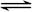 bR(g),温度和压强对该反应的影响如图所示,其中压强p1<p2,由此可判断
bR(g),温度和压强对该反应的影响如图所示,其中压强p1<p2,由此可判断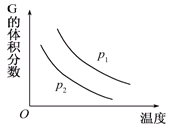
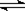 2SO3(g);△H=-Q1 kJ·mol-1,向密闭容器中通入2mol SO2和1mol O2,达到平衡时放出热量Q2KJ,则下列关系式正确的是
2SO3(g);△H=-Q1 kJ·mol-1,向密闭容器中通入2mol SO2和1mol O2,达到平衡时放出热量Q2KJ,则下列关系式正确的是 2HI(g),△H <0,在一带有活塞的密闭容器中达到平衡,
2HI(g),△H <0,在一带有活塞的密闭容器中达到平衡, CO2(g)+H2(g) △H<0 试回答下列问题:
CO2(g)+H2(g) △H<0 试回答下列问题: -1,达到平衡时CO的转化率为60%,则在此温度下,该反应的平衡常数K=
-1,达到平衡时CO的转化率为60%,则在此温度下,该反应的平衡常数K=  大于”、“小于”或“等于”)。
大于”、“小于”或“等于”)。 大”、“减小”或“不变”),
大”、“减小”或“不变”),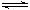 2SO3(g) △H=-197kJ/mol。在25℃时,向恒压密闭容器中通入2 mol SO2和1 mol O2,达到平衡时放出热量a1;若25℃时在此恒压密闭容器中只通入1 mol SO2和0.5 mol O2,达到平衡时放出热量a2。则下列关系正确的是
2SO3(g) △H=-197kJ/mol。在25℃时,向恒压密闭容器中通入2 mol SO2和1 mol O2,达到平衡时放出热量a1;若25℃时在此恒压密闭容器中只通入1 mol SO2和0.5 mol O2,达到平衡时放出热量a2。则下列关系正确的是 2C(g),△H<0。
2C(g),△H<0。