题目内容
9.某饱和一元醛1.5g和足量的银氨溶液发生银镜反应时,生成21.6g银,则该醛是( )| A. | 丙醛 | B. | 丁醛 | C. | 3-甲基丁醛 | D. | 甲醛 |
分析 由RCHO~2Ag可算出此醛的式量为15,各选项均不符合,所以为甲醛,它1mol可以得到4mol银,HCHO~4Ag.
解答 解:n(Ag)=$\frac{21.6g}{108g/mol}$=0.2mol,由RCHO~2Ag可得n(RCHO)=$\frac{1}{2}$×0.2mol=0.1mol,M(RCHO)=$\frac{1.5g}{0.1mol}$=15g/mol,相对分子质量为15,丙醛、丁醛、3-甲基丁醛的相对分子质量均大于15,均不符合,
1mol甲醛可以得到4mol银,HCHO~4Ag,n(HCHO)=$\frac{1}{4}$×0.2mol=0.1mol=0.05mol,M(HCHO)=$\frac{1.5g}{0.05mol}$=30g/mol,相对分子质量为30,因此为甲醛,
故选D.
点评 本题考查醛的有关计算,难度中等,解此题的关键是要知道1mol醛基能还原出2mol银,若醛是甲醛,则lmol醛最多可还原出4mol银.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
15.反应:xA(g)+yB(g)?zC(g),平衡时测得A气体的浓度为0.5mol•L-1,当在恒温下将该容器体积扩大一倍,再次达到平衡,测得A气体的浓度为0.3mol•L-1,下列叙述正确的是( )
| A. | x+y<z | B. | 平衡向右移动 | C. | B的转化率升高 | D. | C的体积分数降低 |
20.已知室温下,0.1mol•L-1某一元酸HA在水中有0.1%发生电离,下列叙述错误的是( )
| A. | HA电离出的c(H+)与水电离出的c(H+)之比为108 | |
| B. | 升高温度,溶液的pH减小 | |
| C. | 溶液的pH=4 | |
| D. | HA的电离平衡常数约为l×10-7 |
17.氧化还原反应在生产、生活中具有广泛的用途,贯穿古今.下列生产、生活中的实例中发生了氧化还原反应的是( )
| A. |  用石斧解剖 | B. |  早期的农业耕作 | C. |  简单机械织布 | D. |  祥云火炬燃烧 |
4.市场上出售的饮料各种各样,有不法商贩为增加饮料口感和粘稠度,在饮料中加塑化剂,塑化剂的分子式为C16H22O4,不能作为食品添加剂.塑化剂属于( )
| A. | 单质 | B. | 氧化物 | C. | 无机物 | D. | 有机物 |
14.下列各选项所述的两个量,前者一定大于后者的是( )
| A. | 同温下分别在100g水中最多能溶解的无水CuSO4和CuSO5•5H2O的质量 | |
| B. | 纯水在25℃和90℃时的pH值 | |
| C. | 25℃时,等体积的pH都等于3的盐酸和AlCl3溶液中,已电离的水分子数 | |
| D. | 在反应NH3+NO→N2+H2O中,被氧化和被还原的N原子数 |
18.羟基扁桃酸是药物合成的重要中间体,它可由苯酚和乙醛酸在一定的条件下反应制得.
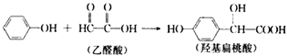
下列有关说法不正确的是( )
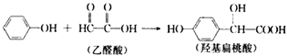
下列有关说法不正确的是( )
| A. | 该反应是加成反应 | |
| B. | 1 mol羟基扁桃酸能与3mol NaOH反应 | |
| C. | 乙醛酸与H2加成的产物能在催化剂作用下形成高分子化合物 | |
| D. | 苯酚和羟基扁桃酸遇上FeCl3溶液都会显色 |
19.化学与社会、科学、技术、环境等有密切关系.下列说法不正确的是( )
| A. | 司母戊鼎、定远舰甲板、有机玻璃等原材料属于合金 | |
| B. | 氯气是塑料、合成橡胶、合成纤维、农药、染料及药品的重要原料 | |
| C. | 工业上生产玻璃、水泥、漂白粉均需要用石灰石为原料 | |
| D. | 用浸泡过溴的四氯化碳溶液的硅藻土吸收水果产生的乙烯以达到保鲜目的 |