题目内容
15.有机物加氢反应中镍是常用的催化剂.但H2中一般含有微量CO会使催化剂镍中毒,反应过程中消除CO的理想做法是投入少量SO2,为搞清该方法对催化剂的影响,查得资料: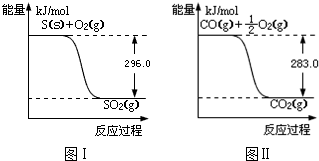
则:①不用通入O2氧化的方法除去CO的原因是避免O2与Ni反应再使其失去催化作用.
②SO2(g)+2CO(g)=S(s)+2CO2(g)△H=-270kJ/mol.
分析 ①Ni能与氧气反应,据此解答即可;
②由图I可知,O2(g)+2CO(g)=2CO2(g)△H=(-2×283)kJ•mol-1=-566kJ•mol-1,(i)
由图II可知,S(s)+O2(g)=SO2(g)△H=-296kJ•mol-1,(ii)
利用盖斯定律进行计算即可.
解答 解:①Ni能与氧气反应,使Ni失去催化作用;
故答案为:避免O2与Ni反应再使其失去催化作用;
②由图I可知,O2(g)+2CO(g)=2CO2(g)△H=(-2×283)kJ•mol-1=-566kJ•mol-1,(i)
由图II可知,S(s)+O2(g)=SO2(g)△H=-296kJ•mol-1,(ii)
(i)-(ii)得:SO2(g)+2CO(g)=S(s)+2CO2(g)△H=-563-(-298)=-270kJ•mol-1,
故答案为:-270kJ/mol.
点评 本题考查了催化剂、盖斯定律的应用,题目难度不大,侧重于考查学生的分析能力和对基础知识的应用能力.

练习册系列答案
 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
5.下列说法正确的是( )
| A. | 金属镁着火时,可用CO2灭火器进行灭火 | |
| B. | 用淀粉碘化钾溶液能区分NO2和溴蒸气 | |
| C. | 通常情况下,氮气的性质很不活泼 | |
| D. | 一氧化氮是一种红棕色气体 |
6.有同学对三种牙膏中的摩擦剂成分进行调査,结果如下表:
试回答下列问题:
(1)上述三种摩擦剂中属于酸性氧化物的是SiO2(填化学式.下同);它与氢氟酸反应的
化学方程式是SiO2+4HF=SiF4↑+2H2O
(2)某品牌的摩擦剂可作胃酸中和剂,该反应的离子方程式为Al(OH)3+3H+=Al3++3H2O
(3)从摩擦剂成分考虑,向该防臭牙膏样品中滴加适量稀硝酸,该反应的化学方程式为CaCO3+2HNO3=CO2↑+H2O+Ca(NO3)2.
| 牙膏品牌 | 某儿童牙膏 | 某防臭牙膏 | 某透明牙膏 |
| 摩擦剂 | 氢氧化铝 | 碳酸钙 | 二氧化硅 |
(1)上述三种摩擦剂中属于酸性氧化物的是SiO2(填化学式.下同);它与氢氟酸反应的
化学方程式是SiO2+4HF=SiF4↑+2H2O
(2)某品牌的摩擦剂可作胃酸中和剂,该反应的离子方程式为Al(OH)3+3H+=Al3++3H2O
(3)从摩擦剂成分考虑,向该防臭牙膏样品中滴加适量稀硝酸,该反应的化学方程式为CaCO3+2HNO3=CO2↑+H2O+Ca(NO3)2.
3.下列有机物分子中可形成顺反异构的是( )
| A. | CH3CH═CHBr | B. | CH3-Cl | C. | CH3C≡CCH3 | D. | CH3CH═C(CH3)2 |
20.次氯酸可用于杀菌消毒,已知25℃时:
①HClO(aq)+OH-(aq)=ClO-(aq)+H2O(1)△H=-Q1kJ•mol-1
②H+(aq)+OH-(aq)=H2O(1)△H=-57.3kJ•mol-1
下列说法正确的是( )
①HClO(aq)+OH-(aq)=ClO-(aq)+H2O(1)△H=-Q1kJ•mol-1
②H+(aq)+OH-(aq)=H2O(1)△H=-57.3kJ•mol-1
下列说法正确的是( )
| A. | 在25℃时,次氯酸的电离方程式及热效应可表示为:HClO(aq)=H+(aq)+ClO-(aq)△H=-(57.3+Q1)kJ•mol-1 | |
| B. | 将20mL 1mol/L HClO与10mL1mol/L NaOH混合后的溶液,一定存在:2c(H+)-2c(OH-)=c(ClO-)-c(HClO) | |
| C. | 将0.2mol/L NaClO 与0.1mol/L HCl等体积混合后的溶液,溶液显碱性,则存在:c(ClO-)>c(Cl-)>c(HClO)>c(OH-) | |
| D. | 已知酸性CH3COOH>HClO,则等浓度CH3COONa和NaClO的混合液中:c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+) |
8.短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示,其中W原子的质子数是其M层电子数的三倍,下列说法不正确的是( )
| X | Y | |||
| Z | W | Q |
| A. | X与Y可形成的化合物在5种以上 | |
| B. | 工业上常常通过电解Z的熔融氧化物的方法来获得Z的单质 | |
| C. | 这五种元素形成的简单离子的半径由大到小为:W>Q>X>Y>Z | |
| D. | W、Q两种元素形成的化合物每种原子最外层都达到了8e-稳定结构 |
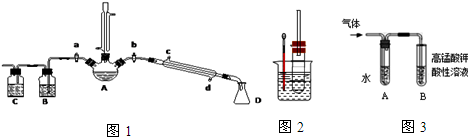
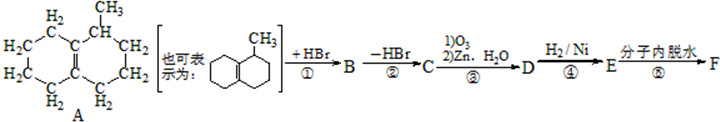 该小组经过上述反应.最终得到F1(
该小组经过上述反应.最终得到F1( )外,还得到它的同分异构体,其中BCDEF分别代表一种或多种物质.
)外,还得到它的同分异构体,其中BCDEF分别代表一种或多种物质.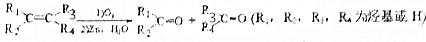
 .
.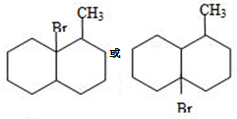 ;
; .
.