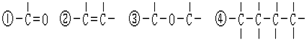题目内容
12.某烧碱样品中含有少量不与酸作用的可溶性杂质,为了测定其纯度,进行以下滴定操作:①在天平上准确秤取烧碱样品W g在烧杯中加蒸馏水溶解;
②用250mL容量瓶配制250mL烧碱溶液;
③用移液管量取25.00mL烧碱溶液于锥形瓶中并加几滴甲基橙指示剂;
④将物质的量浓度为C mol/L的标准H2SO4溶液装入滴定管,调整液面,记下开始刻度数V1mL;
⑤在锥形瓶下垫一张白纸,滴定到终点,记录终点刻度数为V2mL.
回答下面问题:
(1)操作中的锥形瓶下垫一张白纸的作用是便于准确判断终点时颜色的变化情况.
(2)操作中液面应调整到零或零以下某一刻度.
(3)滴定到终点时锥形瓶内溶液的pH约为3.1-4.4,终点时的颜色变化溶液由黄色变为橙色,且半分钟内不恢复为原来的颜色.
(4)若滴定管没有用标准H2SO4溶液润洗,会对测定结果有何影响偏高(填“偏高”“偏低”或“无影响”)(其他操作均正确)
(5)该烧碱样品的纯度计算式是$\frac{0.8C({V}_{2}-{V}_{1})}{W}$×100%.
分析 (1)因锥形瓶下垫一张白纸使滴定终点颜色变化更明显,便于分辨;
(2)滴定管0刻度在上,滴定前应调节到零刻度或零稍下的某一刻度,为减小误差,尖嘴部分应充满液体,无气泡;
(3)指示剂为甲基橙,变色范围为3.1-4.4;
(4)因标准液浓度变小,用量变大;
(5)根据反应消耗的硫酸,求出氢氧化钠,进一步求出样品的纯度.
解答 解:(1)因锥形瓶下垫一张白纸使滴定终点颜色变化更明显,便于分辨,
故答案为:便于准确判断终点时颜色的变化情况;
(2)滴定管0刻度在上,滴定前应调节到零刻度或零稍下的某一刻度,为减小误差,尖嘴部分应充满液体,无气泡,
故答案为:调节到零刻度或零稍下的某一刻度;
(3)指示剂为甲基橙,变色范围为3.1-4.4,终点时pH约为4,溶液由黄色变为橙色,且半分钟内不恢复为原来的颜色;
故答案为:3.1-4.4;溶液由黄色变为橙色,且半分钟内不恢复为原来的颜色;
(4)因标准液浓度变小,用量变大,
故答案为:偏高;
(5)滴到消耗的硫酸为:n(硫酸)=cV=(V2-V1)×10-3L×C mol/L,根据反应方程可知,n(NaOH)=2n(硫酸)=2C(V2-V1)×10-3mol,
所以原来样品中氢氧化钠的物质的量为:2C(V2-V1)×10-3mol×$\frac{250}{25}$=2C(V2-V1)×10-2mol,则样品中氢氧化钠的质量为m(NaOH)=nM=80C(V2-V1)×10-2g,则该烧碱样品的纯度为:$\frac{80C({V}_{2}-{V}_{1})×1{0}^{-2}g}{Wg}$×100%=$\frac{0.8C({V}_{2}-{V}_{1})}{W}$×100%;
故答案为:$\frac{0.8C({V}_{2}-{V}_{1})}{W}$×100%.
点评 本题综合考查酸碱中和滴定,侧重于化学实验基本操作以及物质的含量的测定等问题,题目难度中等,建议在学习中把握相关基本实验方法,学习中注意积累.

| A. | 铝是地壳中含量最多的元素 | B. | 铁是人类冶炼最多的金属 | ||
| C. | 汞是所有金属中熔点最低的 | D. | 钙是人体内最多的金属元素 |
 在“测定1mol气体体积”实验中,我们通常选择的测量气体是氢气,选择的反应原理是镁和稀硫酸反应.
在“测定1mol气体体积”实验中,我们通常选择的测量气体是氢气,选择的反应原理是镁和稀硫酸反应.(1)直接测定H2的体积和质量,操作上比较繁复,我们通常采用转化的思想,即把H2的质量转化成镁带的质量,所以实验中硫酸用过量;把H2的体积转化成所排液体的体积.
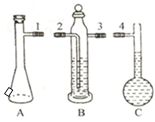
(2)如图中的A、B、C三部分能组成气体摩尔体积测定装置.
A、B、C装置接口的连接顺序是1324.
该装置正确连接后怎样做气密性检查?塞上A(气体发生器)加料口的橡皮塞,B(储液瓶)中导管液面会有所上升,上升的液柱1分钟内不下降,可以确认气密性良好.
本实验中有两次针筒抽气,需要记录的是第2次抽出气体的体积.
(3)这是某同学实验数据的记录:
温度:25℃,气压:101.3kPa
| 实验次数 | 镁带质量(g) | 硫酸体积(mL) | C瓶读数(mL) | 抽出气体的体积(mL) |
| 1 | 0.108 | 10.0 | 129.2 | 8.0 |
| 2 | 0.105 | 10.0 | 125.7 | 6.2 |
实验温度下,1mol氢气的体积的理论值为24.5L,实验误差=14.7%(保留一位小数).
| A. | 尿素 | B. | 乙醇 | C. | 乙酸 | D. | 葡萄糖 |
| A. | 质量为12 g | |
| B. | 体积为22.4 L | |
| C. | 二氧化碳分子个数约为6.02×1023个 | |
| D. | 氧原子个数约为6.02×1023个 |
 表示的有机物,能在一定条件下发生消去反应的共有( )
表示的有机物,能在一定条件下发生消去反应的共有( )| A. | 5 种 | B. | 10种 | C. | 20 种 | D. | 30种 |
| A. | 小苏打中加入过量的澄清石灰水:Ca2++2OH-+2HCO3-═CaCO3↓+2H2O+CO32- | |
| B. | 偏铝酸钠溶液中通入过量的CO2:CO2+3H2O+2AlO2-═2Al(OH)3↓+CO32- | |
| C. | Na2SO3溶液使酸性KMnO4溶液褪色:5SO32-+6H++2MnO4-═5SO42-+2Mn2++3H2O | |
| D. | Fe(NO3)2溶液中加入过量的HI溶液:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O |