题目内容
写出与下列化学方程式相应的离子方程式.
(1)CuCl2+2NaOH=Cu(OH)2↓+2NaCl ;
(2)HCl+NaOH=NaCl+H2O ;
(3)CaCO3+2HCl=CaCl2+H2O+CO2↑ ;
(4)2HCl+Na2CO3=H2O+CO2↑+2NaCl ;
(5)CuCl2+Fe=FeCl2+Cu ;
(6)Ba(OH)2+CuSO4=BaSO4↓+Cu(OH)2↓ .
(1)CuCl2+2NaOH=Cu(OH)2↓+2NaCl
(2)HCl+NaOH=NaCl+H2O
(3)CaCO3+2HCl=CaCl2+H2O+CO2↑
(4)2HCl+Na2CO3=H2O+CO2↑+2NaCl
(5)CuCl2+Fe=FeCl2+Cu
(6)Ba(OH)2+CuSO4=BaSO4↓+Cu(OH)2↓
考点:离子方程式的书写
专题:
分析:(1)只有Cu(OH)2在离子反应中保留化学式;
(2)只有水在离子反应中保留化学式;
(3)难溶物碳酸钙、弱电解质水、气体二氧化碳都写化学式,可溶性强电解质HCl、氯化钙都写离子;
(4)水、二氧化碳在离子反应中保留化学式;
(5)单质用化学式;
(6)BaSO4和Cu(OH)2用化学式.
(2)只有水在离子反应中保留化学式;
(3)难溶物碳酸钙、弱电解质水、气体二氧化碳都写化学式,可溶性强电解质HCl、氯化钙都写离子;
(4)水、二氧化碳在离子反应中保留化学式;
(5)单质用化学式;
(6)BaSO4和Cu(OH)2用化学式.
解答:
解:(1)离子反应为Cu2++2OH-=Cu(OH)2↓,故答案为:Cu2++2OH-=Cu(OH)2↓;
(2)NaOH+HCl=NaCl+H2O的离子反应为H++OH-=H2O,故答案为:H++OH-=H2O;
(3)难溶物碳酸钙、弱电解质水、气体二氧化碳都写化学式,可溶性强电解质HCl、氯化钙都写离子,离子方程式为CaCO3+2H+=Ca2++H2O+CO2↑,故答案为:CaCO3+2H+=Ca2++H2O+CO2↑;
(4)Na2CO3+2HCl=2NaCl+H2O+CO2↑的离子反应为CO32-+2H+=H2O+CO2↑,故答案为:CO32-+2H+=H2O+CO2↑;
(5)离子反应为Cu2++Fe=Fe2++Cu,故答案为:Cu2++Fe=Fe2++Cu;
(6)反应用离子方程式表示为:2OH-+Ba2++Cu2++SO42-=BaSO4↓+Cu(OH)2↓,故答案为:2OH-+Ba2++Cu2++SO42-=BaSO4↓+Cu(OH)2↓.
(2)NaOH+HCl=NaCl+H2O的离子反应为H++OH-=H2O,故答案为:H++OH-=H2O;
(3)难溶物碳酸钙、弱电解质水、气体二氧化碳都写化学式,可溶性强电解质HCl、氯化钙都写离子,离子方程式为CaCO3+2H+=Ca2++H2O+CO2↑,故答案为:CaCO3+2H+=Ca2++H2O+CO2↑;
(4)Na2CO3+2HCl=2NaCl+H2O+CO2↑的离子反应为CO32-+2H+=H2O+CO2↑,故答案为:CO32-+2H+=H2O+CO2↑;
(5)离子反应为Cu2++Fe=Fe2++Cu,故答案为:Cu2++Fe=Fe2++Cu;
(6)反应用离子方程式表示为:2OH-+Ba2++Cu2++SO42-=BaSO4↓+Cu(OH)2↓,故答案为:2OH-+Ba2++Cu2++SO42-=BaSO4↓+Cu(OH)2↓.
点评:本题考查离子反应方程式书写的书写,明确在离子反应中哪些物质应保留化学式及反应的实质是解答本题的关键,难度不大.

练习册系列答案
相关题目
下列装置或操作合理的是( )
A、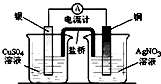 装置可将化学能转化为电能 |
B、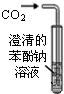 装置可用于比较碳酸、苯酚酸性的强弱 |
C、 装置可用来进行浓硫酸的稀释 |
D、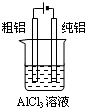 装置可用于电解精炼铝 |
1-丁烯醇(CH2=CH-CH2-CH2OH)可发生的化学反应类型有:( )
①加成 ②氧化 ③酯化 ④加聚 ⑤取代.
①加成 ②氧化 ③酯化 ④加聚 ⑤取代.
| A、①②③④⑤ |
| B、只有①②③ |
| C、只有①②③④ |
| D、只有①③④ |
下列物质的用途中,不正确的是( )
| A、纯碱:制玻璃 |
| B、烧碱:治疗胃酸过多的一种药剂 |
| C、过氧化钠:制氧气 |
| D、小苏打:发酵粉主要成份 |
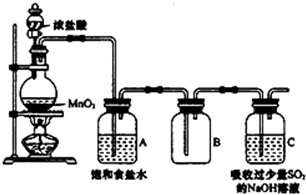 某科研小组用MnO2的浓盐酸制备Cl2时,利用刚吸收过少量SO2的NaOH溶液对尾气进行吸收处理,如图所示:
某科研小组用MnO2的浓盐酸制备Cl2时,利用刚吸收过少量SO2的NaOH溶液对尾气进行吸收处理,如图所示: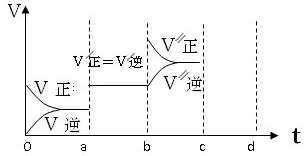 在25℃时,2L的密闭容器中A、B、C三种气体的初始浓度和平衡浓度如下表:
在25℃时,2L的密闭容器中A、B、C三种气体的初始浓度和平衡浓度如下表: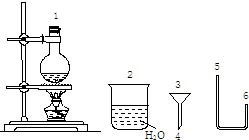 欲配制500mL0.2mol/LNa2CO3溶液,回答下列问题:
欲配制500mL0.2mol/LNa2CO3溶液,回答下列问题: