题目内容
最近科学家提出一种“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使空气中的CO2转变为甲醇.其技术流程如下: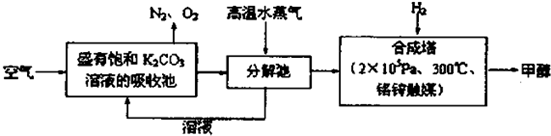
(1)碳酸钾溶液所起的作用是 ;化学方程式为 ;
(2)分解池中发生反应化学方程式为: ;
(3)上述流程中能体现循环利用的物质有 ;
(4)合成塔中生成甲醇的反应,其原子利用率理论上 (能、否)达到100%若合成塔中有2.2kgCO2与足量H2恰好完全反应,可放出2473.5kJ的热量,试写出合成塔中发生反应的热化学方程式 .
(5)如果空气不经过吸收池和分解池,而是直接通入合成塔,你认为 (填“可行”或“不可行”),理由是 .
上述合成反应具有一定的可逆性,从平衡移动原理分析,低温有利于原料气的转化,而实际生产中采用300°C的温度,其原因是 .

(1)碳酸钾溶液所起的作用是
(2)分解池中发生反应化学方程式为:
(3)上述流程中能体现循环利用的物质有
(4)合成塔中生成甲醇的反应,其原子利用率理论上
(5)如果空气不经过吸收池和分解池,而是直接通入合成塔,你认为
上述合成反应具有一定的可逆性,从平衡移动原理分析,低温有利于原料气的转化,而实际生产中采用300°C的温度,其原因是
考点:物质分离和提纯的方法和基本操作综合应用
专题:实验设计题
分析:把空气吹入碳酸钾溶液,碳酸钾会吸收空气中二氧化碳气体,得到碳酸氢钾溶液,在高温水蒸汽中碳酸氢钾分解生成碳酸钾,二氧化碳和水,目的是富集二氧化碳,进入合成塔,通入氢气在一定温度压强下反应生成甲醇;
(1)碳酸钾吸收空气中二氧化碳反应生成碳酸氢钾;
(2)分解池中是碳酸氢钾分解生成碳酸钾、二氧化碳和水;
(3)依据即可以做反应物有做生成物的物质可以循化利用分析;
(4)依据合成甲醇的反应产物分析判断原子利用率,原子利用率是指反应物中的所有原子进入期望产物中的百分比,反应达到完全转化,即100%转化为目标产物;
(5)空气中的氧气和氢气混合加热或点燃可能发生爆炸;依据影响反应速率的因素分析,此温度会提高反应速率,催化剂活性最大;
(1)碳酸钾吸收空气中二氧化碳反应生成碳酸氢钾;
(2)分解池中是碳酸氢钾分解生成碳酸钾、二氧化碳和水;
(3)依据即可以做反应物有做生成物的物质可以循化利用分析;
(4)依据合成甲醇的反应产物分析判断原子利用率,原子利用率是指反应物中的所有原子进入期望产物中的百分比,反应达到完全转化,即100%转化为目标产物;
(5)空气中的氧气和氢气混合加热或点燃可能发生爆炸;依据影响反应速率的因素分析,此温度会提高反应速率,催化剂活性最大;
解答:
解:(1)碳酸钾能和二氧化碳反应生成碳酸氢钠,所以碳酸钾的作用是:吸收空气中二氧化碳,富集空气中的CO2,反应的化学方程式为:K2CO3+CO2+H2O=2KHCO3;
故答案为:富集空气中的CO2,K2CO3+CO2+H2O=2KHCO3;
(2)在加热条件下,碳酸氢钾能分解生成碳酸钾、二氧化碳和水,化学方程式为:2KHCO3
K2CO3+CO2↑+H2O;
故答案为:2KHCO3
K2CO3+CO2↑+H2O;
(3)在吸收池中碳酸钾、水是反应物,在分解池中碳酸钾、水是生成物,所以碳酸钾、水可循环使用;
故答案为:碳酸钾溶液和高温水蒸气;
(4)CO2与H2在300℃、2KPa的条件下生成水和甲醇,化学方程式为:CO2+3H2
H2O+CH3OH,产物有甲醇、还有H2O,不符合转化率100%,若合成塔中有2.2kgCO2与足量H2恰好完全反应,可放出2473.5kJ的热量,1mol二氧化碳反应放热49.47KJ,写出合成塔中发生反应的热化学方程式为:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H=-49.4KJ/mol;
故答案为:否,CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H=-49.4KJ/mol;
(5)如果空气不经过吸收池和分解池,而是直接通入合成塔,空气中的氧气和氢气混合加热或点燃可能发生爆炸,引发危险;依据影响反应速率的因素分析,此温度会提高反应速率,催化剂活性最大;
故答案为:不可以,空气中的氧气和氢气混合加热或点燃可能发生爆炸,提高反应速率,催化剂活性最大;
故答案为:富集空气中的CO2,K2CO3+CO2+H2O=2KHCO3;
(2)在加热条件下,碳酸氢钾能分解生成碳酸钾、二氧化碳和水,化学方程式为:2KHCO3
| ||
故答案为:2KHCO3
| ||
(3)在吸收池中碳酸钾、水是反应物,在分解池中碳酸钾、水是生成物,所以碳酸钾、水可循环使用;
故答案为:碳酸钾溶液和高温水蒸气;
(4)CO2与H2在300℃、2KPa的条件下生成水和甲醇,化学方程式为:CO2+3H2
| ||
故答案为:否,CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H=-49.4KJ/mol;
(5)如果空气不经过吸收池和分解池,而是直接通入合成塔,空气中的氧气和氢气混合加热或点燃可能发生爆炸,引发危险;依据影响反应速率的因素分析,此温度会提高反应速率,催化剂活性最大;
故答案为:不可以,空气中的氧气和氢气混合加热或点燃可能发生爆炸,提高反应速率,催化剂活性最大;
点评:本题考查了甲醇的工业生产,主要考查物质的相互转化和制备的方法及注意事项,在解答时,首先分析题中的转化流程,然后结合学过的知识进行解答,题目难度中等.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与1.344L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸.若向所得硝酸铜溶液中加入 6mol?L-1 NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是( )
| A、60 mL |
| B、40mL |
| C、30 mL |
| D、15 mL |
根据下列三个反应,判断下列物质的氧化性由强到弱的顺序是( )
①2Fe3++2I-=2Fe2++I2
②2Fe2++C12=2Fe3++2C1-
③2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O.
①2Fe3++2I-=2Fe2++I2
②2Fe2++C12=2Fe3++2C1-
③2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O.
| A、Fe3+>C12>MnO4- |
| B、Fe3+>Cl2>I2 |
| C、I2>Cl2>Fe3+ |
| D、MnO4->Cl2>Fe3+ |
反应aA(g)+bB(g)?cC(g)+dD(g),若v (D)=b mol?L-1?s-1,则v (B)为( )
| A、b2 mol?L-1?s-1 | ||
B、
| ||
| C、b mol?L-1?s-1 | ||
| D、db2 mol?L-1?s-1 |