题目内容
9.钠在一定条件下可以在CO2中燃烧生成Na2O和C,下列说法不正确的是( )| A. | 该条件下,钠的还原性强于C | |
| B. | 若CO2过量,则有Na2CO3生成 | |
| C. | 该反应中化学能除转化为热能外,还转化为电能 | |
| D. | Na2O是离子化合物,其中离子半径:r(Na+)>r(O2-) |
分析 Na在二氧化碳中燃烧方程式为4Na+CO2$\frac{\underline{\;点燃\;}}{\;}$2Na2O+C,
A.该反应中Na元素化合价由0价变为+1价、C元素化合价由+4价变为0价,所以Na是还原剂、C是还原产物,同一氧化还原反应中还原剂的还原性大于还原产物的还原性;
B.二氧化碳是酸性氧化物、氧化钠是碱性氧化物,二者发生反应生成盐;
C.该反应中化学能转化为热能,没有转化为电能;
D.氧化钠中只含离子键,电子层结构相同的离子,离子半径随着原子序数增大而减小.
解答 解:Na在二氧化碳中燃烧方程式为4Na+CO2$\frac{\underline{\;点燃\;}}{\;}$2Na2O+C,
A.该反应中Na元素化合价由0价变为+1价、C元素化合价由+4价变为0价,所以Na是还原剂、C是还原产物,同一氧化还原反应中还原剂的还原性大于还原产物的还原性,所以还原性Na>C,故A正确;
B.二氧化碳是酸性氧化物、氧化钠是碱性氧化物,二者发生反应生成盐,所以过量的二氧化碳和氧化钠反应生成碳酸钠,故B正确;
C.该反应中钠燃烧放出热量,没有形成原电池,所以该反应中有化学能转化为热能,没有转化为电能,故C错误;
D.氧化钠由钠离子和氧离子构成,为离子化合物,电子层结构相同的离子,离子半径随着原子序数增大而减小,所以离子半径:r(Na+)<r(O2-),故D错误;
故选CD.
点评 本题以钠为载体考查氧化还原反应、基本概念、能量转化、元素周期律等知识点,为高频考点,明确基本概念、元素周期律内涵等知识点是解本题关键,知道离子半径大小比较方法,题目难度不大.

练习册系列答案
相关题目
17.下列说法正确的是( )
| A. | 溶液中水的离子积常数(KW)随溶液浓度的改变而改变 | |
| B. | 一般情况下,一元弱酸HA的Ka越大,表明该酸的酸性越弱 | |
| C. | 对已达到化学平衡的反应,改变压强,平衡常数(K)一定改变 | |
| D. | Ksp只与难溶电解质的性质和温度有关,而与溶液中的离子浓度无关 |
4.下列有关说法错误的是( )
| A. | 邻二甲苯属于芳香烃,它的官能团是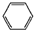 | |
| B. | 分子结构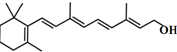 是维生素A的键线式 是维生素A的键线式 | |
| C. | 氯溴碘代甲烷的同分异构体数目有两个,就像人的左右手似的 | |
| D. | 乙醇与二甲醚互为同分异构体,这种同分异构现象叫官能团异构 |
14.下列说法正确的是( )
| A. | 按系统命名法的名称为2-甲基-3,5-二乙基乙烷 | |
| B. | 用Na2CO3溶液能区分CH3COOH、CH3CH2OH,苯、硝基苯四种物质 | |
| C. | 等质量的甲烷、乙烯、1,3-丁二烯分别充分燃烧,所耗氧气的量依次增加 | |
| D. | 下列物质的沸点按由低到高顺序为:CH3(CH2)2CH3<(CH3)3CH<CH3(CH2)3CH3 |
1.下列有关分液操作的叙述正确的是 ( )
| A. | 应选用球形分液漏斗进行分液,使用前要检查是否漏水 | |
| B. | 将混合液倒入分液漏斗,塞紧玻璃塞,上下振荡 | |
| C. | 混合液摇匀后,立即将分液漏斗放在铁圈上静置,分层 | |
| D. | 打开分液漏斗的玻璃塞,再打开旋塞,使下层液体从分液漏斗下端放出,待下层液体完全流出后关闭旋塞,把上层液体从分液漏斗上口倒出 |
6. 将海水淡化与浓缩海水资源化结合起来是综合利用海水的重要途径之一.一般是先将海水淡化获得淡水,再从剩余的浓缩海水中通过一系列工艺流程提取其他产品.
将海水淡化与浓缩海水资源化结合起来是综合利用海水的重要途径之一.一般是先将海水淡化获得淡水,再从剩余的浓缩海水中通过一系列工艺流程提取其他产品.
回答下列问题:
(1)采用空气吹出法从浓海水中吹出Br2,并用纯碱吸收.碱吸收溴的主要反应是Br2+Na2CO3+H2O→NaBr+NaBrO3+NaHCO3(未配平),吸收1molBr2时,转移的电子为$\frac{5}{3}$mol.
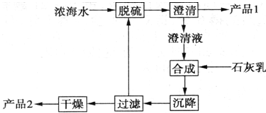
(2)海水提镁的一段工艺流程如下图:
浓主要成分如下:
产品2的化学式为Mg(OH)2,1L浓海水最多可得到产品2的质量为69.6g.
(3)采用石墨阳极、不锈钢阴极电解熔融的氯化镁,发生反应的化学方程式为MgCl2(熔融)$\frac{\underline{\;通电\;}}{\;}$ Mg+Cl2↑,电解时,若有少量水存在会造成产品镁的消耗,写出有关的化学方程式Mg+2H2O$\frac{\underline{\;高温\;}}{\;}$ Mg(OH)2+H2↑.
 将海水淡化与浓缩海水资源化结合起来是综合利用海水的重要途径之一.一般是先将海水淡化获得淡水,再从剩余的浓缩海水中通过一系列工艺流程提取其他产品.
将海水淡化与浓缩海水资源化结合起来是综合利用海水的重要途径之一.一般是先将海水淡化获得淡水,再从剩余的浓缩海水中通过一系列工艺流程提取其他产品.回答下列问题:
(1)采用空气吹出法从浓海水中吹出Br2,并用纯碱吸收.碱吸收溴的主要反应是Br2+Na2CO3+H2O→NaBr+NaBrO3+NaHCO3(未配平),吸收1molBr2时,转移的电子为$\frac{5}{3}$mol.
(2)海水提镁的一段工艺流程如下图:
浓主要成分如下:
| 离子 | Na+ | Mg2+ | Cl- | SO42- |
| 浓度/(g•L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
(3)采用石墨阳极、不锈钢阴极电解熔融的氯化镁,发生反应的化学方程式为MgCl2(熔融)$\frac{\underline{\;通电\;}}{\;}$ Mg+Cl2↑,电解时,若有少量水存在会造成产品镁的消耗,写出有关的化学方程式Mg+2H2O$\frac{\underline{\;高温\;}}{\;}$ Mg(OH)2+H2↑.
7.室温时,某溶液中由水电离生成的H+和OH-物质的量浓度的乘积为1×10-24,则在该溶液中一定不能大量共存的离子组是( )
| A. | Al3+、Na+、NO3-、Cl- | B. | K+、Na+、Cl-、CO32- | ||
| C. | Mg2+、Na+、Cl-、SO42- | D. | NH4+、K+、SiO32-、NO3- |
