题目内容
下列与有机物的结构、性质有关的叙述正确的是( )
| A、用新制氢氧化铜悬浊液无法鉴别葡萄糖和乙酸 |
| B、乙酸与乙醇可以发生酯化反应,又均可与碳酸氢钠溶液反应 |
| C、硫酸铵、硫酸铜和乙醇均能使蛋白质变性 |
| D、二氯甲烷不存在同分异构体 |
考点:有机物的结构和性质,有机物的鉴别,同分异构现象和同分异构体,乙醇的化学性质,乙酸的化学性质,氨基酸、蛋白质的结构和性质特点
专题:同分异构体的类型及其判定,有机物的化学性质及推断
分析:A.葡萄糖和乙酸分别与氢氧化铜悬浊液反应的现象为:砖红色沉淀、蓝色溶液;
B.乙酸中含-COOH,具有酸性,酸性比碳酸强;
C.硫酸铵使蛋白质发生盐析;
D.甲烷为正四面体结构,四个H相同,均为相邻位置.
B.乙酸中含-COOH,具有酸性,酸性比碳酸强;
C.硫酸铵使蛋白质发生盐析;
D.甲烷为正四面体结构,四个H相同,均为相邻位置.
解答:
解:A.葡萄糖和乙酸分别与氢氧化铜悬浊液反应的现象为:砖红色沉淀、蓝色溶液,现象不同,可鉴别,故A错误;
B.乙酸中含-COOH,具有酸性,酸性比碳酸强,则乙酸与乙醇可以发生酯化反应,与碳酸氢钠溶液反应,但乙醇、乙酸乙酯与碳酸氢钠不反应,故B错误;
C.硫酸铵使蛋白质发生盐析,而硫酸铜和乙醇均能使蛋白质变性,故C错误;
D.甲烷为正四面体结构,四个H相同,均为相邻位置,则二氯甲烷只有一种结构,不存在同分异构体,故D正确;
故选D.
B.乙酸中含-COOH,具有酸性,酸性比碳酸强,则乙酸与乙醇可以发生酯化反应,与碳酸氢钠溶液反应,但乙醇、乙酸乙酯与碳酸氢钠不反应,故B错误;
C.硫酸铵使蛋白质发生盐析,而硫酸铜和乙醇均能使蛋白质变性,故C错误;
D.甲烷为正四面体结构,四个H相同,均为相邻位置,则二氯甲烷只有一种结构,不存在同分异构体,故D正确;
故选D.
点评:本题考查有机物的结构与性质,为高频考点,涉及结构中官能团的性质、有机物的鉴别、蛋白质性质及同分异构体分析等,注重基础知识的考查,题目难度不大.

练习册系列答案
相关题目
有机化合物A转化为B的反应如下,下列说法正确的是( )
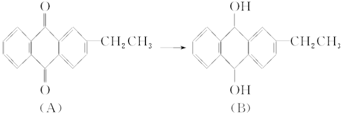

| A、B的分子式为C16H14O2 |
| B、上述转化属于还原反应 |
| C、二者均为芳香烃 |
| D、二者均能发生加成、酯化反应 |
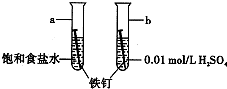 如图是研究铁钉腐蚀的装置图.下列说法不正确的是( )
如图是研究铁钉腐蚀的装置图.下列说法不正确的是( )| A、ab在两处的腐蚀速率a<b |
| B、a、b两处铁钉中的碳均为正极 |
| C、a、b两处铁钉中的铁均失电子被氧化 |
| D、a、b两处的正极反应式均为O2+4e-+4H+═2H2O |
下列说法正确的是( )
| A、有化学键断裂的过程一定发生化学变化 | ||
| B、氯化钠是一种电解质,电解饱和食盐水可制得金属钠 | ||
C、将pH=a的醋酸稀释为pH=a+1的过程中,
| ||
| D、SiO2是酸性氧化物,能与强碱溶液反应,但不与任何酸反应 |
下列说法正确的是( )
| A、0.1mol/L溶液中的(NH4)2SO4溶液中的c(NH4+)<c(SO42-) |
| B、相同温度下,0.6mol/L氨水溶液与0.3 mol/L氨水溶液中c(OH-)之比是2:1 |
| C、向0.1mol/L NaNO3溶液中滴加硝酸使溶液pH=5,此时混合液中的c(Na+)<c(NO3-) |
| D、向醋酸钠溶液中加入适量醋酸,使混合液pH=7,此时混合液中c(Na+)<c(CH3COO-) |
以氧化铝为原料制取氢氧化铝,最好的方法是( )
| A、将氧化铝溶于水 |
| B、将氧化铝先溶于盐酸中,之后滴加氨水 |
| C、将氧化铝溶于盐酸中,之后滴加氢氧化钠溶液 |
| D、将氧化铝溶于氢氧化钾 |
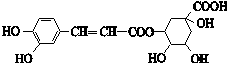 下列有关绿原酸(结构简式如图)的说法不正确的是( )
下列有关绿原酸(结构简式如图)的说法不正确的是( )| A、分子式为C16H18O9 |
| B、1mol绿原酸最多能与8mol NaOH反应 |
| C、1mol绿原酸最多能与4mol H2反应 |
| D、能发生取代反应、消去反应、加成反应和氧化反应 |
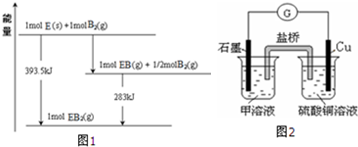
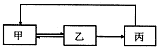 下表中各组物质之间不能通过一步反应实现如图转化的是( )
下表中各组物质之间不能通过一步反应实现如图转化的是( )