题目内容
某有机物结构简式为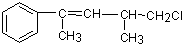 ,关于该有机物叙述不正确的是( )
,关于该有机物叙述不正确的是( )
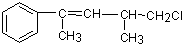 ,关于该有机物叙述不正确的是( )
,关于该有机物叙述不正确的是( )| A、不能使酸性KMnO4溶液褪色 |
| B、能使溴水褪色 |
| C、在加热和催化剂作用下,最多与4 mol H2反应 |
| D、能发生水解反应 |
考点:有机物的结构和性质
专题:有机物的化学性质及推断
分析:由结构简式可知,分子中含双键、-Cl,结构烯烃和卤代烃的性质来解答.
解答:
解:A.含双键,能使酸性KMnO4溶液褪色,故A错误;
B.含双键,能使溴水褪色,故B正确;
C.苯环与双键均与氢气发生加成反应,则在加热和催化剂作用下,最多与4 mol H2反应,故C正确;
D.含-Cl,在NaOH溶液中能发生水解反应生成醇,故D正确;
故选A.
B.含双键,能使溴水褪色,故B正确;
C.苯环与双键均与氢气发生加成反应,则在加热和催化剂作用下,最多与4 mol H2反应,故C正确;
D.含-Cl,在NaOH溶液中能发生水解反应生成醇,故D正确;
故选A.
点评:本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重烯烃、卤代烃性质的考查,题目难度不大.

练习册系列答案
相关题目
下列做法不利于能源“开源节流”的是( )
| A、大力开采煤、石油、天然气以满足人们日益增长的能源需求 |
| B、在农村地区开发沼气能源,将废弃的秸秆转化为清洁高效的能源 |
| C、开发太阳能、水能、风能、地热等新能源、减少使用煤、石油等化石燃料 |
| D、减少私家车数量,大力发展公共交通 |
用NaHCO3和KHCO3组成的混合物分别与三份相同浓度的盐酸进行反应,测得数据如下:
判断下列结论中不正确的是( )
| 50mL盐酸 | 50mL盐酸 | 50mL盐酸 | |
| m(混合物) | 9.2g | 15.7g | 27.6g |
| V(CO2)(标准状况) | 2.24L | 3.36L | 3.36L |
| A、混合物中NaHCO3和KHCO3的质量比为1:1 |
| B、加入9.2g混合物时消耗HCl 0.1mol |
| C、盐酸物质的量浓度为3.0mol/L |
| D、15.7g混合物与盐酸反应后有剩余 |
等质量的下列物质充分燃烧消耗氧气最多的是( )
| A、CH4 |
| B、C2H2 |
| C、C3H6 |
| D、C2H4 |
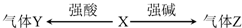 X、Y、Z均为中学化学常见物质,在一定条件下,X能与强酸或强碱溶液发生如图的反应(部分反应物、生成物及反应条件略去).则下列说法不正确的是( )
X、Y、Z均为中学化学常见物质,在一定条件下,X能与强酸或强碱溶液发生如图的反应(部分反应物、生成物及反应条件略去).则下列说法不正确的是( )| A、若X为金属单质,则Y、Z可能为同一物质 |
| B、若X为盐,则Y在标况下的密度一定是1.96g?L-1 |
| C、若X为盐,则Z一定能使湿润的红色石蕊试纸变蓝 |
| D、若X为正盐,则其水溶液中水的电离程度比同温度下纯水的电离程度大 |
下列反应中,属于加成反应的是( )
| A、SO3+H2O=H2SO4 | ||||
B、CH2=CH2+H2O
| ||||
C、CH3Cl+Cl2
| ||||
| D、CO2+2NaOH=Na2CO3+H2O |
3.9g镁铝合金恰好完全溶解于120mL4mol/L的盐酸中,再加入60mL8mol/L的氢氧化钠溶液,得到沉淀10.7g,则加入盐酸时产生氢气的物质的量为(mol)( )
| A、0.17 | B、0.18 |
| C、0.20 | D、0.21 |
如图是元素周期表中碘元素的部分信息,下列说法正确的是( )


| A、碘元素的质量数为53 |
| B、碘元素的相对原子质量是126.9 |
| C、碘原子最外层有7个能量相同的电子 |
| D、碘原子的5p亚层有3个成对电子 |
某同学欲配制含有大量下列各离子的溶液,其中能实现的是( )
A、Fe3+、NH
| ||
B、K+、H+、SO
| ||
C、Fe2+、Fe3+、Na+、NO
| ||
D、Fe2+、NH
|