题目内容
下列离子方程式正确的是( )
| A、溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+═AgBr↓ |
| B、漂白粉溶液中通入足量的SO2气体:Ca2++2ClO-+SO2+H2O═CaSO-3↓+2HClO |
| C、KHSO4熔融状态下电离:KHSO4=K++H++SO42- |
| D、CH3COOH是弱电解质:CH3COO-+H2O?CH3COOH+OH- |
考点:离子方程式的书写
专题:离子反应专题
分析:A.硝酸银溶液和自由移动的卤素离子发生离子反应;
B.二者反应生成硫酸钙、硫酸和盐酸;
C.硫酸氢钾在熔融状态下电离生成钾离子和硫酸氢根离子;
D.醋酸根离子水解生成醋酸和氢氧根离子.
B.二者反应生成硫酸钙、硫酸和盐酸;
C.硫酸氢钾在熔融状态下电离生成钾离子和硫酸氢根离子;
D.醋酸根离子水解生成醋酸和氢氧根离子.
解答:
解:A.硝酸银溶液和自由移动的卤素离子发生离子反应,溴乙烷中不含自由移动的溴离子,所以不能直接用硝酸银溶液检验溴元素,故A错误;
B.二者反应生成硫酸钙、硫酸和盐酸,离子方程式为2SO2+Ca2++2ClO-+2H2O=4H++2Cl-+CaSO4↓+SO42-,故B错误;
C.硫酸氢钾在熔融状态下电离生成钾离子和硫酸氢根离子,离子方程式为KHSO4=K++HSO4-,故C错误;
D.醋酸为弱酸,水解离子方程式为CH3COO-+H2O?CH3COOH+OH-,故D正确;
故选D.
B.二者反应生成硫酸钙、硫酸和盐酸,离子方程式为2SO2+Ca2++2ClO-+2H2O=4H++2Cl-+CaSO4↓+SO42-,故B错误;
C.硫酸氢钾在熔融状态下电离生成钾离子和硫酸氢根离子,离子方程式为KHSO4=K++HSO4-,故C错误;
D.醋酸为弱酸,水解离子方程式为CH3COO-+H2O?CH3COOH+OH-,故D正确;
故选D.
点评:本题考查了离子方程式、电离方程式及水解方程式的书写,明确物质的性质是解本题关键,易错选项是B、C,注意B中能发生氧化还原反应,C在硫酸氢钾在水溶液里和熔融状态下电离方程式的区别,为易错点.

练习册系列答案
 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
下列说法中正确的是( )
| A、在101kPa时,1mol物质完全燃烧时所放出的热量,叫做该物质的燃烧热 |
| B、酸和碱发生中和反应生成1mol水,这时的反应热叫中和热 |
| C、等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
| D、由单质A转化为单质B,△H=+119KJ/mol,可知单质A比单质B稳定 |
以下物质中与1一丁烯不是同系物的是( )
| A、乙烯 | B、2一甲基一2一丁烯 |
| C、环丙烯 | D、2一丁烯 |
以下是一些常用的危险品标志,装运乙醇的包装箱应贴的图标是( )
A、 腐蚀品 |
B、 爆炸品 |
C、 有毒气体 |
D、 易燃液体 |
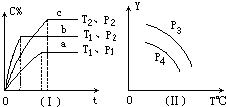 在某容积一定的密闭容器中,可逆反应:A(g)+B(g)?xC(g),符合下列图象(Ⅰ)所示关系.由此推断对图(Ⅱ)的正确说法是( )
在某容积一定的密闭容器中,可逆反应:A(g)+B(g)?xC(g),符合下列图象(Ⅰ)所示关系.由此推断对图(Ⅱ)的正确说法是( )| A、p3>p4,Y轴表示A的质量 |
| B、p3>p4,Y轴表示混合气体平均摩尔质量 |
| C、p3>p4,Y轴表示混合气体密度 |
| D、p3<p4,Y轴表示B的百分含量 |
下列实验基本操作(或实验注意事项)中,主要是出于实验安全考虑的是( )
| A、可燃性气体的验纯 |
| B、过滤时玻璃棒不能在漏斗内搅拌 |
| C、使用分液漏斗前要检验是否漏液 |
| D、滴管不能交叉使用 |
下列各对物质中,不是互为同系物的是( )
A、环己烷与  |
B、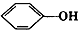 和 和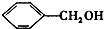 |
| C、甲苯和二甲苯 |
| D、乙酸和硬脂酸 |