题目内容
写出下列反应的离子方程式:
(1)钠投入水中:
(2)氢氧化铁中加入稀硫酸:
(3)氯化铵溶液中加入氢氧化钾溶液:
(4)澄清的石灰水中加入足量的碳酸氢钠溶液: .
(1)钠投入水中:
(2)氢氧化铁中加入稀硫酸:
(3)氯化铵溶液中加入氢氧化钾溶液:
(4)澄清的石灰水中加入足量的碳酸氢钠溶液:
考点:离子方程式的书写
专题:
分析:(1)反应生成NaOH和氢气;
(2)反应生成硫酸铁和水;
(3)反应生成氯化钾和一水合氨;
(4)反应生成碳酸钠、碳酸钙、水.
(2)反应生成硫酸铁和水;
(3)反应生成氯化钾和一水合氨;
(4)反应生成碳酸钠、碳酸钙、水.
解答:
解:(1)反应生成NaOH和氢气,离子反应为2Na+2H2O=2Na++2OH-+H2↑,故答案为:2Na+2H2O=2Na++2OH-+H2↑;
(2)反应生成硫酸铁和水,离子反应为Fe(OH)3+3H+=Fe3++3H2O,故答案为:Fe(OH)3+3H+=Fe3++3H2O;
(3)反应生成氯化钾和一水合氨,离子反应为NH4++OH-
NH3?H2O,故答案为:NH4++OH-
NH3?H2O;
(4)反应生成碳酸钠、碳酸钙、水,离子反应为2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O,故答案为:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O.
(2)反应生成硫酸铁和水,离子反应为Fe(OH)3+3H+=Fe3++3H2O,故答案为:Fe(OH)3+3H+=Fe3++3H2O;
(3)反应生成氯化钾和一水合氨,离子反应为NH4++OH-
| ||
| ||
(4)反应生成碳酸钠、碳酸钙、水,离子反应为2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O,故答案为:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O.
点评:本题考查离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应及复分解反应的离子反应考查,题目难度中等.

练习册系列答案
相关题目
早在1807年化学家戴维用电解熔融氢氧化钠制得钠,反应原理为:4NaOH(熔融)=4Na+O2↑+2H2O;后来盖?吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH=Fe3O4+2H2↑+4Na↑.下列有关说法不正确的是( )
| A、电解熔融氢氧化钠制钠,阴极发生电极反应为:Na++e-=Na |
| B、盖?吕萨克法制钠原理是利用铁的还原性比钠强 |
| C、若戴维法与盖?吕萨克法制得等量的钠,则两反应中转移的电子总数比为1:2 |
D、目前工业上常用电解熔融氯化钠法制钠(如图),电解槽中石墨极为阳极,铁为阴极 |
下列关于胶体的叙述不正确的是( )
| A、利用丁达尔现象可以区别溶液和胶体 |
| B、胶体都可以发生丁达尔现象 |
| C、胶体粒子的大小都在1nm-100nm之间 |
| D、加热氢氧化铁胶体没有明显现象 |
C12摩尔质量为( )
| A、71g | B、71 |
| C、71g/mol | D、71mol |
想一想,如果将Ba(OH)2(固体)、CuSO4(固体)、纯醋酸(液态)归为一类,下列物质还可以和它们归为一类的是( )
| A、硝酸钠晶体 |
| B、豆浆 |
| C、Fe (OH)3胶体 |
| D、75%的酒精溶液 |

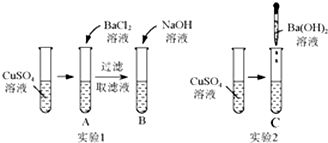 仔细分析如图中的实验:
仔细分析如图中的实验: